RNA viruses negative strand and double strand
DNA VIRUSES
The Influenza Virus
کاشف2
پینل(پزشک)
فیلیپ پینل پزشک فرانسوی بسال 1745 متولد شد ودر سال 1826 در گذشت. وی پزشک عالیقدری بود ودر اثر تحقیقاتی که درباره جنون وبیماریهای روانی نموده بود طریق جدیدی برای مداوا وجلوگیری انواع واقسام ناراحتی های روحی پیدا کرد.
لوفر(میکروبشناس)
فردریک لوفر(F.LOFFER) (1852-1915) میکروبشناس آلمانی است که در سال 1880 موفق به کشف میکروب بیماری دیفتری گردید.
لیستر(پزشک)
ژوزف لیستر(Lister) (1912- 1827) طبیب وجراح انگلیسی که برای نخستین بار اکتشافات پاستور دربارهء میکروب را در جراحی مورد استفاده قرارداد. یعنی اهمیت ضدعفونی کردن آلات وافزار جراحی برای مبارزه با میکرب را گوشزد نمود.
نوکوچی(دانشمند)
هیده یونوکوچی (1928-1876) باکترولوژیست ژاپنی که سرم آبله کوبی را اختراع و راه های تازه در درمان بیماری سیفلیس را پیدا کرد.
منبع: زندگینامه معروفترین دانشمندان ومخترعان جهان (مهرداد مهرین)
وبا؛ بیماری از قدیم تا حال

آوارگی جمعیتهای انسانی بر اثر جنگ، همیشه زمینهساز بروز و همهگیر شدن بیماری وبا در مناطق گوناگون جهان بوده است.
کابوس «وبا» در حوزه ادبیات
«وبا» از دوران کهن، سایه ی وهمناک خود را بر زندگی نسلهای انسانی افکنده است.
طغیان «وبا» در دورههایی از تاریخ، قربانیان بیشماری برجای گذاشته و هراس از این بیماری، تا حوزه شعر و قصه و ادبیات ملتها دامن کشیده است. نمونههایی از اشعار شاعران ایرانی وجود دارد که به گونهای در آنها خطر وبا، به صورت نمادین مطرح شده است. بد نیست بدانید که نام «عشق سالهایی وبایی» بر یکی از آثار معروف «گابریل گارسیا مارکز» نویسنده بزرگ آمریکای لاتین ماندگار شده است و نمایانگر این واقعیت است که زنجیره وبا، به صورت یک دور تسلسل باطل در کره مسکونی ما قربانی گرفته است و در آستانه سده بیست و یکم، همچنان در صدر دشمنان سلامتی بشر قرار دارد.
به همین دلیل سازمان جهانی بهداشت، تلاشهای خود را برای گسستن این زنجیره به کار گرفته است تا با ایمنسازی تدریجی مناطق وباخیز، راه مهار و ریشه کنی این بیماری مرگ بار تاریخ بشر را هموار کند.
تلاش جهانی برای قطع زنجیره «وبا»
بیماری وبا، در فصل مساعد سال و در ایران در اردیبهشت ماه امکان بروز و شیوع پیدا میکند و منحنی شیوع بیماری در تابستان اوج میگیرد و با فرا رسیدن پاییز دامنه انتشار بیماری کاهش یافته و در ماه آذر به صفر میرسد.
پایان شیوع بیماری در ماه میانی پاییز به منزله نابودی میکروب این بیماری نیست، بلکه میکروبها همانطورکه اشاره شد تا درجات معینی از سرما نیز در زمستان زنده میمانند و در بهار سال بعد دوباره چرخه بروز و شیوع بیماری از سرگرفته میشود. بنابراین رعایت بهداشت در تمام زمینهها میتواند نقش مهمّی در مهار این بیماری داشته باشد.
نشانههای بیماری وبا
اسهال و استفراغ از نشانههای بیماری وباست. در اسهال وبایی گاهی رشتههای سفید نیز دیده میشود. این نوع اسهال به هیچ وجه اسهال خونی نیست و در بسیاری موارد در حد خفیف و متوسط است. در صورت عارض شدن بیماری شدید بیمار درد شکم ندارد و مدفوع آبکی و جاری است. با شدت گرفتن اسهال ظرف چند ساعت بیمار به اغماء میرود و اگر به موقع به یک مرکز درمانی رسانده نشود، جان خود را از دست میدهد. بنابراین کاهش شدید آب بدن علت اصلی مرگ بیمار وبایی است. افراد به محض مشاهده این نشانهها باید به مرکز بهداشتی و بیمارستانی مراجعه کنند و با دادن آزمایش (در صورت نوع متوسط) بستری شوند.

چرخه انتقال بیماری
انتقال فرد به فرد در بیماری وبا وجود ندارد و دست زدن به بیمار مثل ایدز یا هپاتیت اشکالی ندارد و بیماری از این طریق انتقال نمییابد. تنها راه انتقال این بیماری از طریق مدفوع فرد مبتلا میباشد.
آشامیدن آبهای آلوده بهویژه در فصل گرما برای رفع تشنگی، استفاده از آبهای آبیاری درختان برای شست و شوی میوهها، خرید انواع خوراکیهای خام و بستنی از دستفروشان و مصرف یخ آلوده امکان انتقال میکروب بیماریهای رودهای و اسهالی مثل "وبا" را افزایش می دهد. بنابراین کوتاه کردن مرتب ناخنها برای جلوگیری از تجمع آلودگی در زیر آنها، شست وشوی مرتب دستها با آب و صابون پس از توالت، شستن کاهو و سبزیجات با آب سالم و ضدعفونیکردن آنها با مایع ظرفشویی یا ضدعفونی کننده، جوشاندن کشک مایع و شیر پاستوریزه نشده و دفع مناسب زبالهها میتواند این چرخه انتقال را متوقف کند.
آشنایی مسئولان و کارکنان یک مرکز درمانی، از دربان گرفته تا پزشک معالج میتواند در درمان و نجات بهموقع یک بیمار حاد وبایی مؤثر واقع شود.
بیماری باید ظرف 48 ساعت توسط مسئولین وزارت بهداشت به سازمان بهداشت جهانی اطلاع داده شود. اما متأسفانه روند اطلاع رسانی به سازمان بهداشت جهانی، اکنون توسط کشورها رعایت نمیشود. دلیل این مورد نیز برخوردهای نامناسب سیاسی و اقتصادی با کشور درگیر این نوع بیماریهاست. بههمین جهت کشورها از ترس تحریم اقتصادی ترجیح میدهند این نوع موارد را گزارش ندهند.
شبکه مراقبت بیماریهای همهگیر
مراقبت به معنی استفاده به موقع و صحیح از اطلاعات مربوط به وقایعی است که ثبت و جمعآوری شده و در یک مرکز طبقهبندی میشود. براساس این اطلاعات شاخصهای بهداشتی مشخص میشود و نقاط قوت و ضعف یک بیماری و مسائل بهداشتی، تعیین و امکان اصلاح و مبارزه با بیماری فراهم میشود. در واقع مجموع اطلاعات بهدست آمده بهصورت گزارش مستند به مسئولان مربوطه برای اصلاح و بهبود شاخصهای بهداشتی ارائه میشود تا اقدامات مقتضی صورت پذیرد.
نظام مراقبت بیماریهای همهگیر، یک نظام پیوسته است که از مراکز بهداشتی کشورها شروع و به مرکز سازمان بهداشت جهانی ختم میشود. چگونگی برخورد با بیماریهای همهگیر متفاوت است. در جایی که بیماری اسهال آبکی حاد در افراد 5 سال به بالاتر مشاهده شد نیازی به آزمایش نیست و باید به وبا مشکوک شد و مراقبتهای بهداشت و درمان را آغاز کرد. مردم آنقدر باید با تعاریف بیماری وبا آشنا باشند که خودشان با مشاهده نشانهها بلافاصله به مرکز بهداشتی منطقه گزارش دهند.
پیامهای بهداشتی صریح نیست
به اعتقاد کارشناسان بهداشتی پنهان کردن اخبار بهداشتی به مصلحت هیچکس و هیچجا نیست. این نکته بهویژه در مرزهای داخلی یک کشور، اهمیت بیشتری به خود میگیرد، زیرا علاوه بر زیانهای اقتصادی و سیاسی، جان انسانها را نیز به خطر میاندازد.
افراد بهدلیل عدم اطلاع کافی از بروز یک بیماری، مبتلا میشوند و جانشان به خطر میافتد. بی تردید مسأله بیماری وبا نیز بهعنوان بیماری بومی ایران، مسئولیت دستگاههای مرتبط امور بهداشتی را دوچندان میکند و ارائه اطلاعات همگانی و آموزش فراگیر از طریق رسانههای جمعی بهویژه صدا و سیما میتواند در کاهش این بیماری موثرتر واقع شود.
یک خانم خانهدار در این مورد میگوید: چندی پیش از طریق تلویزیون و در برنامههای مختلفی راجع به رعایت اصول بهداشتی در استفاده از سبزی و میوه و آب بهداشتی اطلاعاتی کسب کردم که بهصورت ابهامآمیزی نیز امکان ابتلا به بیماریهای واگیردار را گوشزد میکرد امّا اعلام مستقیم و هشدارهای به موقع گویا چندان مورد توجّه مسئولان نیست.
به اعتقاد کارشناسان پنهان کردن اطلاعات و اخبار مربوط به شیوع بیماریهای همهگیر که با جان شماری از انسانها سرو کار دارد ،هر نوع مصلحتاندیشی مسئولان را تحتشعاع قرار داده و زیر سوال میبرد. بنابراین اطلاعات شفاف و بهموقع تنها راه حل منطقی است.
منبع:http://www.tebyan.net
معرفی محیط TSIدر باكتري شناسي

| H2S | Sucrose | Lactose | Glucose |
Slant/Butt/Gas |
|
- |
- |
- |
- |
Red/Red/None |
|
- |
- |
- |
A |
Red/Yellow/None |
|
- |
- |
- |
AG |
Red/Yellow/Gas |
|
- |
? |
AG |
AG |
Yellow/Yellow/Gas |
|
+ |
AG |
- |
AG |
Yellow/Black/Gas |
|
+ |
- |
- |
AG |
Red/Black/Gas |
رودولف لوكارت
رودولف لوكارت Rudolph Leuckartبعنوان پدر انگلشناسى و نيز يكى از مشهورترين جانورشناسان قرن نوزدهم شناخته ميشود. لوكارت با نام كامل كارل گئورگ رودولف لوكارت Karl Georg Friedrich Rudolf Leuckart در سال 1822 در شهر Helmstedt آلمان بدنيا آمد. در جوانى زمانى كه دانشجوى پزشكى بود به جانورشناسى علاقه پيدا كرد و تحت هدايت جانورشناس مشهور رودولف واگنر Rudolph Wagner به مطالعه پرداخت. در 1852 بعنوان دانشجوى ممتاز و بخاطر تزش از دانشگاه جايزه گرفت. او اندكى پس از گرفتن دكتراى پزشكى MD از دانشگاه گوتينگن آلمان، دوره جانورشناسى را با سفر علمى به درياى شمال براى مطالعه بيمهرگان دريايى آغاز كرد. توصيف دقيق او از جزئيات مرفولوژيك كمك بزرگى براى رشته جديدالتاسيس سيستماتيك جانورى بود؛ ايدهاى مبتنى بر اينكه با توجه به تغييرات ساختارى ميتوان تكامل را رديابى كرد. لوكارت در 1845 (28 سالگي) به درجه استاديارى و در 1869 به استاد كاملى دانشگاه لايپزيگ نايل شد. او در سال 1898 درگذشت. معروفترين كارهاى لوكارت در زمينه انگل شناسى بر عفونتهاى مهره داران، بويژه تنياها، فاسيولا و تريشين و پنتاستوميا متمركز بود. او نشان داد كه تنيا ساژيناتا فقط در گاو و تنيا سوليوم فقط در خوك رخ ميدهد. او به كمك همكارش چرخه زندگى تريشين در خوك و انسان را مستند كرد. كتابهاى درسى لوكارت امروزه قديمى و كلاسيك هستند. او معلم برجستهاى بود و نمودارهاى ديوارى علمى (Wall Chart) تهيه كرد و از آنها در تدريس كمك ميگرفت. در سال 1892 بيش از صد تن از شاگردان او بمناسبت 70 سالگى لوكارت، نمايشگاهى از اين چارتها تشكيل دادند.
منبع:http://parasitology.wordpress.com
اثر حفاظتی گروه خونی O در مالاريای وخیم
 در طول تاریخ بشر، مالاریا همواره یک نیروی انتخاب طبیعی عمده بوده است و چندین پلیمرفیسم گلبولهای قرمز را پدید آورده است که انسان را در برابر مالاریای وخیم مقاوم میکند. تشکیل رزت (حالت گلسرخیشدن گلبولهای قرمز؛ یک فنوتیپِ ویرولانس انگل که با مالاریای وخیم همراه است؛ شكل روبرو) در گلبولهای گروه خونی O، در مقایسه با گلبولهای گروههای خونی A، B و AB کمتر دیده میشود. با وجود این، تاکنون توجه کمی به نقش سیستم گروه خونی ABO در محافظت انسانها بر علیه مالاریای وخیم شده است. گروهی از محققان این فرضیه را مطرح کردهاند که گروه خونی O میتواند از طریق مکانیسمِ کاهشِ تشکیل رزت، موجب مقاومت در برابر مالاریای فالسیپاروم وخیم شود. آنها در یک مطالعه شاهد- موردیِ جورشده روی ۵۶۷ کودک اهل کشور مالی دریافتند که گروه خونی O، تنها در ۲۱ درصد موارد وخیم مالاریا وجود داشت، در حالیکه نسبت این گروه خونی در مبتلایان به مالاریای عادی و افراد سالم، حدود ۴۵ درصد بود. به علاوه شانس گسترش مالاریای وخیم در افراد دارای گروه خونی O در مقایسه با ساير گروههای خونی، ۶۶ درصد کمتر بود. در همین افراد مورد مطالعه، تشکیل رزت در ایزولههای انگلی حاصل از کودکان با گروه خونی O در مقایسه با ایزولههای حاصل از کودکان دارای گروههای خونی غیر O، کمتر بود. آنالیز آماری نشان داد که بین گروه خونی ABO میزبان و فراوانی تشکیل رزت توسط انگل، ارتباط معنیداری وجود دارد که از فرضیه آنها مبنی بر اثر حفاظتی گروه خونی O از طریقِ مکانیسمِ کاهشِ تشکیلِ رزت توسط پلاسمودیوم فالسیپارم، حمایت میکند. این تحقیق به روشن شدن بیشترِ پاتوژنز مالاریا کمک میکند و حاکی از آن است که فشارِ انتخابی ناشی از مالاریا میتواند در توزیع جهانی گروههای خونی ABO در جمعیتهای انسانی دخالت داشته باشد.
در طول تاریخ بشر، مالاریا همواره یک نیروی انتخاب طبیعی عمده بوده است و چندین پلیمرفیسم گلبولهای قرمز را پدید آورده است که انسان را در برابر مالاریای وخیم مقاوم میکند. تشکیل رزت (حالت گلسرخیشدن گلبولهای قرمز؛ یک فنوتیپِ ویرولانس انگل که با مالاریای وخیم همراه است؛ شكل روبرو) در گلبولهای گروه خونی O، در مقایسه با گلبولهای گروههای خونی A، B و AB کمتر دیده میشود. با وجود این، تاکنون توجه کمی به نقش سیستم گروه خونی ABO در محافظت انسانها بر علیه مالاریای وخیم شده است. گروهی از محققان این فرضیه را مطرح کردهاند که گروه خونی O میتواند از طریق مکانیسمِ کاهشِ تشکیل رزت، موجب مقاومت در برابر مالاریای فالسیپاروم وخیم شود. آنها در یک مطالعه شاهد- موردیِ جورشده روی ۵۶۷ کودک اهل کشور مالی دریافتند که گروه خونی O، تنها در ۲۱ درصد موارد وخیم مالاریا وجود داشت، در حالیکه نسبت این گروه خونی در مبتلایان به مالاریای عادی و افراد سالم، حدود ۴۵ درصد بود. به علاوه شانس گسترش مالاریای وخیم در افراد دارای گروه خونی O در مقایسه با ساير گروههای خونی، ۶۶ درصد کمتر بود. در همین افراد مورد مطالعه، تشکیل رزت در ایزولههای انگلی حاصل از کودکان با گروه خونی O در مقایسه با ایزولههای حاصل از کودکان دارای گروههای خونی غیر O، کمتر بود. آنالیز آماری نشان داد که بین گروه خونی ABO میزبان و فراوانی تشکیل رزت توسط انگل، ارتباط معنیداری وجود دارد که از فرضیه آنها مبنی بر اثر حفاظتی گروه خونی O از طریقِ مکانیسمِ کاهشِ تشکیلِ رزت توسط پلاسمودیوم فالسیپارم، حمایت میکند. این تحقیق به روشن شدن بیشترِ پاتوژنز مالاریا کمک میکند و حاکی از آن است که فشارِ انتخابی ناشی از مالاریا میتواند در توزیع جهانی گروههای خونی ABO در جمعیتهای انسانی دخالت داشته باشد.
منبع:http://parasitology.wordpress.com
کاشف
برزیل(طبیب)
دکتر ویتال برزیل از اطبای مشهور معاصر برزیل است که برای نخستین بار سرم ضد زهر مار را کشف کرد.
برنارد(پزشک)
کلودبرنارد(1813-1878) از علمای وظائف الاعضاء فرانسوی بود ووظیفه پانکراس و یا لوزالمعده در هضم مواد روغنی وظیفه کبد در تکوین قند کبدی را کشف کرد.
برینگ (دانشمند)
امیل فن برینگ (Behring) بسال 1854 توانست برای نخستین بار سرم دیفتری بسازد. برینگ بسال 1917در گذشت.
پاولوف (فیزیولوژیست)
ایوان پتروویچ پاولوف، از شخصیتهای بزرگ علمی روس در سال 1849 بدنیا آمد ودر 1936 در گذشت. بمناسبت کارهایی که در فیزیولوژی دستگاه گوارش انجام داده بود بسال 1904 بوی جایزهء نوبل اعطاء گردید.
منبع: زندگینامه معروفترین دانشمندان ومخترعان جهان (مهرداد مهرین)
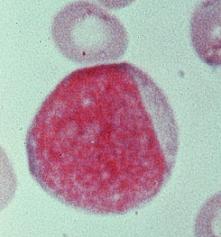
دفاع بدن
 |
|
|
دفاع سطحی
دفاع مکانیکی
یک نوع آن مانعی است که پوست برای ورود میکروبها ایجاد میکند. در صورتی که بدن به هر دلیلی خراشیده یا شکننده شود، میکروبها به سادگی امکان عبور از آن را خواهند داشت. بدی تغذیه ، دود سیگار ، آلودگی هوا و امثال آن میتوانند باعث ضعیف شدن و شکنندگی پوست شوند. گرد و غبار ذرات موجود در هوا غالبا حامل میکروبهایی هستند که عامل عفونتهای دستگاه تنفساند. سرفه و عطسه نیز دو عمل مکانیکی دیگرند که ذرات و مواد خارجی و نیز میکروارگانیسمها را به خارج میرانند.اعتیاد به الکل کلیه واکنشهای دفاعی مکانیکی را تضعیف کرده و موجب ورود ذرات خارجی و میکروبها به داخل ششها میشود که در نتیجه میتواند موجب ذاتالریه گردد. موهای سطحی بدن و نیز جریان ادرار و اشک موجب کنده شدن و شسته شدن میکروبها از بینی ، مجاری ادراری و چشمهای میشوند. جدا شدن یاختههای مرده از پوست به نحوی موثر بسیاری ازمیکروبهای متصل به یاختههای پوششی را بیرون میریزد. همه بافت پوششی دستگاه گوارش در مدت 36 ساعت بطور کامل تعویض میشود.
دفاع شیمیایی
ترشحات مخاطی ، اشک ، عرق و آب دهان همگی حاوی آنزیمی به نام لیزوزیم هستند که دیواره یاختهای بسیاری از باکتریها را حل میکند. اسیدهای چرب موجود در عرق و ترشحات گوارشی دارای خواص ضدباکتری و قارچ هستند و معده حاوی اسید کلریدریک غلیظ است که میتواند سرعت میکروبها را از بین ببرد. آب دهان ، علاوه بر آنزیم لیزوزیم ، دارای یک سیستم دفاعی ضدمیکروبی اضافی هست که سیستم لاکتوپراکسیداز نامیده میشود.دفاع میکروبی
باکتریهای بومی سطح پوست میتوانند از طریق رقابت بر سر مواد غذایی ، تغییر شرایط محیطی مانند PH و ترشح ترکیبات متابولیسمی ویژه با میکروارگانیسمهای بیماریزا مقابله کرده و از رشد آنها جلوگیری کنند. مثلا لاکتو باسیلها که معمولا در مهبل افراد بالغ یافت میشوند، مولد اسید لاکتیک هستند این امر موجب کاهش PH مهبل تا حدود 4 و 4.5 میشود که برای اکثر میکروبهای بیماریزا قابل تحمل نیست.دفاع به روش بیگانه خواری
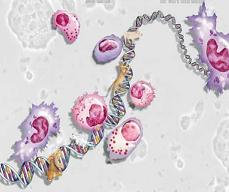 |
یاختههای بیگانهخوار
یکی از ویژگیهای گروهی از گویچههای سفید خون ، به نام گرانوسیتها وجود لیزوزومها در این یاختههاست. فراوانترین نوع گرانولوسیت موجود در خون نوتروفیلها هستند که به دلیل داشتن هسته چند گرهی لوکوسیت نیز خوانده میشوند. نوتروفیلها از نظر بیگانهخواری بسیار فعالاند و معمولا اولین یاختههای محافظی هستند که خود را به منطقه عفونی میرسانند عمر این یاختهها کوتاه است. آگرانولوسیتها شامل لنفوسیتها و مونوسیتها هستند. مونوسیتها در بافتها جای میگیرند و به ماکروفاژ تبدیل میشوند. ماکروفاژها عمدتا به صورت چسبیده به بافتهای جگر، طحال، غدههای لنفاوی ، مغز استخوان و رگهای خونی و لنفاوی یافت میشوند.این هیستوسیتها مانند صافی عمل میکنند و ذرات مختلف موجود در خون و لنف را به هنگام عبور از این بخشها در محاصره میگیرند و بدینترتیب عوامل بالقوه بیماریزا را به دام میاندازند. ماکروفاژهای سرگردان به ششها ، طحال و سایر نقاطی که ممکن است میکروبها در آنها یافت شوند میروند. همچنین ماکروفاژها به مناطق عفونی رفته و در واکنش حفاظتی کلی بیمار شرکت میکنند. مونوسیتها و ماکروفاژها شبکهای به نام رتیکولوآندوتلیال را بوجود میآورند که در مرحله حاد یا مزمن بیماری نقش دارد.
التهاب و تورم
بافتهای بدن جانوران در مقابل برخی از محرکهای خارجی و عفونت ، از طریق التهاب واکنش نشان میدهند که قرمزی ، تورم ، گرما و درد از ویژگیهای آن است. اثر اولیه محرک خارجی گشاد شدن رگهای خون و افزایش نفوذپذیری رگهای مویین است. این امر منجر به افزایش جریان خون و خارج شدن مایعات از دستگاه گردش خون و ورود آنها به بافتها میشود که به تورم و التهاب میانجامد. یکی از عوامل موثر در شروع واکنش التهابی ، مادهای شیمیایی به نام هیستامین است که توسط یاختههای آسیب دیده آزاد شده و موجب افزایش نفوذپذیری رگهای مویین میشود.ایمنی
سومین نوع دفاع بدن ، دفاع ایمنی است که شامل ایمنی یاختهای و ایمنی عمومی (هومورال) است.- ایمنی: نوع ویژهای از مقاومت است که اولا در طول زندگی فرد بر اثر تماس با مواد خارجی مشخص ایجاد میشود ثانیا اغلب تنها در برابر یک نوع میکروب بیماریزا باهم که محرک تولید آن بوده است نقش حفاظتی دارد ثالثا موجب حفاظت در برابر عامل محرک ایمنی برای مدت طولانی است.
- پادگن: هر مادهای که بطور اختصاصی واکنشی ایمنی ویژهای را پس از ورود به بدن موجب گردد. پادگن (آنتی ژن) نامیده میشود. پادگنها از پروتئین یا پلی ساکارید تشکیل شدهاند که حاوی نقاط شیمیایی مشخص به نام شاخصهای پادگن است که ویژگیهای آن را تعیین میکند پادگنها میتوانند محرک ایمنی عمومی و ایمنی با واسطه یاختهای باشند.
 |
ایمنی عمومی
از آنجا که این ایمنی وابسته به مولکولهای مشخصی به نام پادتن است و در مایعات بدن (هوموس) قابلحل است هومورال نامیده میشود. با ورود یک پادگن به بدن ، پادتن تولید میگردد که قادر به ایجاد پیوند اختصاصی با پادگن محرک تولید آن است. پادتنها تحت نام کلی ایمونوگلوبولین نیز شناخته میشوند زیرا ، جز گروهی از پروتئینها به نام گلوبولینها هستند. ایمونوگلوبولینها بر مبنای خواص فیزیکی ، شیمیایی و ایمونولوژیکی به 5 گروه عمده:IgE ، IgD ، IgG ، IgM ، IgA تقسیم میشوند. ایمونوگلوبولینها با وجود تنوع ساختاری اغلب از چهار رشته پروتئینی تشکیل شدهاند که به شکل ساختار Y به یکدیگر پیوند یافتهاند. دو رشته کوتاهتر را رشته یا زنجیرههای سبک (L) مینامند که با پیوند کووالانس به انشعابات رشته یا زنجیره های درازتر سنگین متصل میشوند اختصاصی بودن نقاط اتصال به وسیله ترتیب قرار گرفتن امینواسیدها در بخش متغیر هر دو رشته L و H تعیین میشود. تعداد نقاط اتصال بر روی پادتن تعیین کننده ظرفیت آن است. پادتن در اثر ترکیب با پادگن میکروبی آن را غیرفعال کرده و یا از انتشار آن در بدن جلوگیری میکند و به انواع پادتنها تقسیم میشوند.
- پادتنهای خنثی کننده: این گروه با ویروسها یا توکسینهای میکروبی واکنش میدهند و اثرات زیانبخش آنها را خنثی میکنند.
- آگلوتینینها: این گروه شامل پادتنهایی است که با پادگنهای ذرهای واکنش نشان میدهند و موجب به هم چسبیدن و تجمع آنها میشوند.
- پرسیپیتینها: این گروه شامل ایمونوگلوبولینهایی است که با پادگنهای محلول واکنش و آنها را به رسوبات جامد تبدیل میکنند.
- اوپسونینها: این گروه شامل پادتنهایی است که با اجزا سطحی یاختههای میکروبی و غیرمیکروبی ترکیب و محرک بلعیده شدن آنتیژنهای مربوط بوسیله یاختههای بیگانهخوار هستند.
- پادتنهای تثبیت کننده مکمل: این گروه از پادتنها یاختههای میکروبی را در حضور یک سری از پروتئینهای خون به نام مکمل متلاشی میکنند. مکملها به همراه پادتنها در سه نوع عمل حفاظتی دخالت دارند: متلاشی شدن ، جذب شیمیایی و اپسونیزاسیون. کل این فرآیند را تثبیت مکمل مینامند.
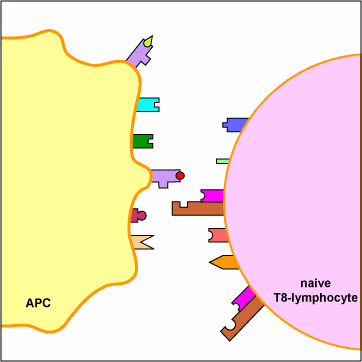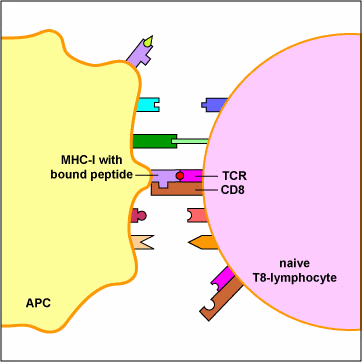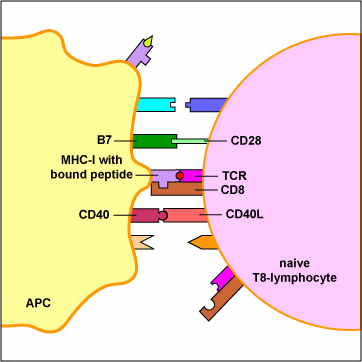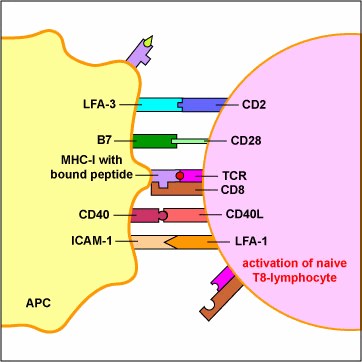 |
|
|
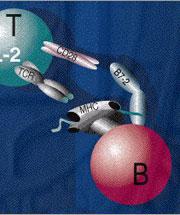
ایمنی با واسطه یاختهای (CMT)
در این نوع ایمنی عمومی با واسطه یاختههای ویژهای به نام لنفوسیتهای T تامین میشود یاختههای T با عبور از تیموس در ایمنی با واسطه یاختهای شرکت میکنند. یاختههای T مولد پادتن نیستند، ولی میتوانند به روش زیر یاختههای بدن را محافظت کنند. نقاط پذیرنده در سطح یاختههای T پادگنهای ویژهای را شناسایی کرده و به آنها متصل میشوند. این اتصال موجب فعال شدن یاختههای T و تحریک آنها به تکثیر میشود و این امر به تشکیل تودهای از لنفوسیتهای ایمنیزا در نقاطی که محل تراکم پادگنهاست میانجامد.
منبع:http://daneshnameh.roshd.i
ایمنی در برابر انگلها
مقدمه
انگل به موجود زندهای اطلاق میشود که در داخل یا خارج بدن موجود دیگری زیست میکند و زندگی خود را از وجود آن حیوان تامین میکند. زندگی انگلی عبارتست از یکی از اشکال همزیستی فیزیولوژیکی بین دو حیوان از دو جنس مختلف که یکی از آنها (انگل) معمولا کوچکتر و ضعیفتر بوده و در سطح یا داخل بدن جنس قویتر (میزبان) زندگانی و تغذیه میکند و در بدن او ایجاد اختلال مینماید. این همزیستی ممکن است دائمی یا موقت باشد.
طبقه بندی انگلهای انسانی
تک سلولی
ماستیگوفورا: تاژکدارانی که یک یا چند تاژک شلاقی دارند و یا در بعضی گونهها دارای غشای مواج هستند. مثل تریپانوزوما.
سارکودینا: آمیبی شکل میباشد مثل انتامبا.
اسپوروزوآ: دارای چرخه زندگی پیچیده با دو مرحله متناوب تولید مثل جنسی و تولید مثل غیر جنسی میباشند. این دو مرحله معمولا نیاز به دو میزبان مختلف دارد. مثل کوکسیدیا و هماتوزوآ.
سیلوفورآ: تک سلولیهای پیچیدهای هستند که بدن آنها دارای مژههایی به صورت ردیفی یا تکهای است و در هر تک سلول ، 2 نوع هسته وجود دارد مثل بالانتیدیوم کلی.
کرمها
کرمهای پهن: سطح پشتی- شکمی تخت هستند و شامل دو رده سستودا و ترماتودا میباشند.
کرمهای گرد یا نخی شکل: کرمهایی با دو جنسیت مجزا و غیر بندبند شامل بسیاری از گونههای انگل انسان هستند مثل فوکونما.
رابطه بیماریهای انگلی و آب و هوا
برخی از بیماریها از تماس مستقیم بیمار با شخص سالم ایجاد میشود مانند امراض ریوی ، آبله ، سرخک و مخملک و یا آنکه در اثر تماس شخص سالم با مدفوع بیمار تولید میشود مانند تب تیفوئید و آمیباز. درحالیکه بعضی از عفونتها برای رسیدن به انسان باید توسط میزبان واسط و یا ناقل بیماری انتقال یابند و چون اکثرا ناقلین در درجه حرارت مناسبی قادر به زیست و تکثیر هستند.
انتشار اینگونه بیماریها محدود به مناطقی است که شرایط جوی و اقلیمی برای رشد و تکثیر میزبان واسط مساعد باشد. در ضمن شدت بیماری به وضع بهداشتی سکنه و قدرت تحمل آنها بستگی دارد و مشاهده میشود که اکثر بیماریهای انگلی در مناطق گرمسیر و در کشورهایی دیده میشود که وضع بهداشت محیط افراد خوب نبوده و در ضمن به واسطه شدت گرما تحمل سکنه به بیماریها کمتر میباشد.
ایمنی در بیماریهای انگلی
استفاده از روشهای ایمنی برای پیشگیری بیماریهای انگلی بسیار کمتر از استفاده از این روشها در بیماریهای ناشی از باکتریها بوده است. در سالهای اخیر در مورد یکی از بیماریهای انگلی که مربوط به بیماری کرمی ششها در دامها میباشد با تهیه واکسن از نوزادهای کرم که در مقابل اشعه مخصوص قرار گرفتهاند نوعی ایمنی حاصل شده است. از علل عدم پیشرفت در استفاده از روشهایایمونولوژی در بیماریهای انگلی آنست که:
اولا برخلاف باکتریها ، کشت انگل در آزمایشگاه به سهولت امکانپذیر نیست و ثانیا در اغلب انگلها بخصوص کرمها ، انگل در داخل بدن انسان در جریان رشد و نمو تغییر شکل میدهد و محل خود را تغییر میدهند و از آنجا که بین توقف انگل در داخل نسوج و ایجاد ایمنی رابطهای مستقیم موجود است شک نیست که میزان ایمنی نسبت به انواع مختلف کرمها بر حسب مدت توقف آنها در نسوج بدن فرق میکند. مثلا ایمنی حاصله از آلودگی به کرم آسکاریس بیشتر در زمانی ایجاد میشود که لارو مرحله مهاجرت ریوی خود را طی مینماید.
نتیجه ایمنی نسبت به انگلها
از تعداد انگل در اعضای بدن حیوان ایمن شده، کاسته میشود.
انگل در بدن آنها رشد کافی ننموده و اغلب به شکل نارس موجود میباشد.
نقصان قدرت تکثیر و تخمگذاری.
کاهش قدرت مهاجرت داخل احشا.
ایجاد تغییرات فیزیولوژیکی و متابولیسم مواد شیمیایی.
از پدیدههای دیگر ایمنی در بیماریهای انگلی ایجاد واکنشهای حساسیت در اثر ورود برخی از انگلها به بدن میباشد. مثلا ابتلا به عفونت آسکاریس در اطفال ممکن است با تظاهرات آلرژی مانند کهیر و خارش و آسم همراه باشد. تزریق داخل جلدی آنتی ژن برخی کرمها به افراد مبتلا به عفونت همان کرم یا کرمهای دسته مشابه سبب ایجاد واکنش جلدی میشود که از آن برای تشخیص بیماری استفاده میکنیم. تظاهر مهم دیگر ایجاد ائوزینوفیلی در اثر ابتلا به انگلها میباشد که از علایم مشخصه ابتلای اکثر انگلها است.
انواع ایمنی در برابر انگلها
محافظت و عدم تماس با منبع آلودگی
ممکن است سکنه یک ناحیه به علت عوامل طبیعی و آب و هوا اصولا در معرض آلودگی یک بیماری نباشند. مثلا سکنه روستاهای اطراف تهران به علت فقدان امکانات برنج کاری و عوامل طبیعی اصولا در معرض آلودگی به کرمهای قلابدار (جزء کرمهای منتقله از راه خاک) نیستند. عامل دیگر که سبب محافظت از ابتلا به بیماری میشود عادات مردم است. مثلا نخوردن گوشت خوک در بین مسلمین ، مانع ابتلا به کرم تریشین میشود.
مقاومت
بعضی از میزبانان نسبت به برخی از انگلها مقاومند. مثلا سیاهپوستان به کرم قلابدار. نیز ممکن است شخص به تعداد معینی انگل مبتلا نشود اما اگر در مجاورت تعداد بیشتری انگل قرار گیرد مبتلا شود. عوامل مقاومت در برابر انگل به صورت زیر است.
شیره معده که موجب منهدم شدن تخم و لارو کرمها میشود
. فقدان مواد لازم برای پرورش انگل.
رژیم غذایی مناسب میزبان ، مانع آلودگی بوسیله انگل میشود.
هر چه سن میزبان بیشتر باشد از نسبت و شدت آلودگی کاسته میشود.
ایمنی اکتسابی
در اثر ورود انگل به میزبان به بدن با مواد حاصله از آن ایجاد میشود. یعنی وجود پادتن که در بدن انسان در اثر وجود آنتی ژن انگلها ایجاد میشود. این نوع ایمنی اختصاصی بوده و فقط نسبت به آن نوع انگل میباشد که وارد بدن شده است. اگر وجود یک نوع انگل در بدن انسان ایجاد ایمنی نسبت به انوع انگل مشابه بکند آن را ایمنی متقاطع گویند. مصونیت به انگلها کامل نمیباشد و ممکن است با از بین رفتن انگل از بدن انسان ، کاهش یافته یا از بین برود مثل مصونیت حاصله در مالاریا.
تشخیص بیماریهای انگلی
بر پایه تغییرات ایمنی در بدن انجام میشود که اساس اکثر آزمایشات ، بر اتصال آنتی ژن با پادتن تولید شده در بدن میباشد و از آزمایشات اصلی دیگر ، آزمون جلدی میباشد که با تزریق جلدی آنتی ژن به فرد مشکوک ، اگر واکنش جلدی رخ دهد فرد بیمار خواهد بود و دیگری هموآگلوتیناسیون میباشد که آنتی ژن همراه اریتروسیت یک حیوان مثل گوسفند را به فرد مشکوک تزریق میکنیم. در صورت وجود پادتن گلبولهای قرمز (اریتروسیت ها) آگلوتینه میشوند.
BACTERIA

Coxiella burnetii

Legionella pneumophila

Staphylococcus aureus

Vibrio cholerae
منبع:http://library.thinkquest.org
Clostridium perifingens

منبع:http://library.thinkquest.org
Salmonella

منبع:http://library.thinkquest.org
تاموکسیفن بر علیه لیشمانیازیس
 محققانی از دانشگاه سائوپولو برزیل توانستهاند کاربرد جدیدی برای داروی قدیمی تاموکسیفن (tamoxifen) پیدا کنند. آنها تاثیر و کارآیی این دارو بر علیه لیشمانیا آمازوننسیس (L. amazonensis)،عامل لیشمانیازیس جلدی در آمریکای جنوبی را ثابت کردهاند. آنها در مقاله خود توضیح میدهند که چگونه تاموکسیفن، دارویی که در سطحی وسیع در درمان و پیشگیری از سرطان پستان استفاده میشود، بر علیه این بیماری انگلی در موشهای آلوده آزمایشگاهی میجنگد. انگلهایی تکسلولی از جنس لیشمانیا عامل ایجادکننده بیماری لیشمانیازیس هستند. درمان لیشمانیازیس مستلزم مصرف داروهای سمی با درجه تحمل پایین است. با توجه به اینکه قبلاً مشخص شده بود که تاموکسیفن به صورت برونتنی (in vitro) بر علیه انگلها فعال هستند، این نویسندگان اکنون کارآیی این دارو را در یک مدل موشی عفونت لیشمانیا آمازوننسیس نشان دادهاند. این گروه از محققان برزیلی در موشهایِ آلودهای که به مدت دو هفته با با تاموکسیفن درمان شده بودند ، کاهش معنیداری در بارِ انگلی مشاهده کردند. همچنین آنها متوجه تاخیر چشمگیری در ایجاد زخمهای پوستی شدند که یک علامت معمول این بیماری است.
محققانی از دانشگاه سائوپولو برزیل توانستهاند کاربرد جدیدی برای داروی قدیمی تاموکسیفن (tamoxifen) پیدا کنند. آنها تاثیر و کارآیی این دارو بر علیه لیشمانیا آمازوننسیس (L. amazonensis)،عامل لیشمانیازیس جلدی در آمریکای جنوبی را ثابت کردهاند. آنها در مقاله خود توضیح میدهند که چگونه تاموکسیفن، دارویی که در سطحی وسیع در درمان و پیشگیری از سرطان پستان استفاده میشود، بر علیه این بیماری انگلی در موشهای آلوده آزمایشگاهی میجنگد. انگلهایی تکسلولی از جنس لیشمانیا عامل ایجادکننده بیماری لیشمانیازیس هستند. درمان لیشمانیازیس مستلزم مصرف داروهای سمی با درجه تحمل پایین است. با توجه به اینکه قبلاً مشخص شده بود که تاموکسیفن به صورت برونتنی (in vitro) بر علیه انگلها فعال هستند، این نویسندگان اکنون کارآیی این دارو را در یک مدل موشی عفونت لیشمانیا آمازوننسیس نشان دادهاند. این گروه از محققان برزیلی در موشهایِ آلودهای که به مدت دو هفته با با تاموکسیفن درمان شده بودند ، کاهش معنیداری در بارِ انگلی مشاهده کردند. همچنین آنها متوجه تاخیر چشمگیری در ایجاد زخمهای پوستی شدند که یک علامت معمول این بیماری است.
نتایج امیدوارکننده این مطالعه به همراه این حقیقت که بیخطری و نمایه داروشناسی تاموکسیفن در انسانها به خوبی تثبیت شده است ( این دارو از دهه ۱970 تاکنون در درمان سرطان پستان استفاده میشود)، نویددهنده یک آلترناتیو در درمان لیشمانیازیس باشد.
منبع:http://parasitology.wordpress.com
Parasitology
مشاهده انگلهای خونی
مواد و وسایل مورد نیاز : 1)الکل متیلیک مطلق 2)رنگ گیمسا 3)میکروسکوپ نوری 4)لام 5)روغن سدر
روش آزمایش
پس از تهیه گسترش از عروق انتهایی گوش آن را کنار گذاشته تا در مجاورت هوا خشک شود .با استفاده از متانول 96 درجه گسترش را Fix می کنیم .بعد از خشک شدن رنگ گیمسا ی غلیظ را به نسبت 1 به 20 با آب مقطر رقیق نموده و روی لام می ریزیم .بعد از 20 دقیقه (بسته به غلظت رنگ ) لام را شسته وبعد از خشک شدن یک قطره روغن سدر روی لام ریخته زیر میکروسکوپ با درشتنمایی ((x 100 مشاهده می نماییم .بسته به بیماری ایجاد شده بابزیا ،تیلریا ،آناپلاسما ،پیروپلاسما و تریپانوزوم قابل روئیت می باشد.
مشاهده تک یاخته های روده ای
مواد و وسایل مورد نیاز: 1)لام 2)لامل 3)میکروسکوپ نوری 4)روغن سدر 5)سرم فیزیولوژی
روش آزمایش
روش تشخيص زردي
تهیه گسترش از غدد لنفاوی
مواد و وسایل مورد نیاز : 1)لام 2) الکل متیلیک مطلق 3) رنگ گیمسا 4) میکروسکوپ نوری 5) روغن سدر
روش آزمایش : از غدد لنفاوی نمونه مشکوک به زردی گسترش تهیه کرده و بعد از خشک شدن
با الکل متیلیک مطلق لام را Fix کرده وبعد از خشک شدن رنگ گیمسا روی لام می ریزیم در صورت بروز بیماری شیزونت انگل قابل روئیت می باشد
آزمایش لورچ
مواد و وسایل مورد نیاز :1)ترازوی دیجیتالی 2)سود 10 درصد (10 گرم سود خالص به حجم 100 ) 3)اتر 4)لوله آزمایش 5) شعله
روش آزمایش
طرز تهیه رنگ گیمسا
مواد و وسایل مورد نیاز :1) پودر گیمسا 2)الکل متیلیک 3)گلیسرین
3.8گرم پودر گیمسا را در 125 میلی لیتر گلیسرین حل کرده ،375 میلی لیتر الکل متیلیک را به آن اضافه می نماییم .
شمارش تخم انگل EPG
شمارش تخم انگل نماتودها
روش آزمایش
3 گرم مدفوع را وزن کرده در هاون چینی می کوبیم ،سپس 42 میلی لیتر آب به طور یکنواخت به آن اضافه نموده محتویات حاصله را با الک 100 صاف کرده و لوله آزمایش را از محتویات صاف شده پر می کنیم .با سرعت 1500 دور به مدت 2 دقیقه سانتریفیوژ می نماییم .(حجم لوله سانتریفوژ 15 میلی لیتر می باشد که حاوی یک گرم نمونه است ) سپس مایع رویی را خالی نموده و با ضربه به ته لوله رسوب را جدا کرده و به رسوب محلول آب شکر اشباع یا آب نمک اشباع اضافه کرده تا لبریز گردد. یک عدد لامل روی لوله قرار داده به مدت 2 دقیقه با سرعت 1000 دور سانتریفیوژ می نماییم .لامل را برداشته روی لام قرار داده و زیر میکروسکوپ با درشتنمایی 10 x شمارش می نماییم در این روش تخم سستودها نیز قابل شمارش می باشد.
شمارش تخم انگل ترماتودها
مواد و وسایل مورد نیاز: 1) مدفوع 2)الک 100 3) هاون چینی 4)آب شکر اشباع یا آب نمک اشباع 5)لام 6) لامل 7)سانتریفوژ 8) لوله آزمایش 9)میکروسکوپ
ابتدا 3 گرم مدفوع را وزن کرده و50-40 میلی لیتر آب اضافه نموده با الک 40 یا چای صاف کن محتویات را صاف شده را در لوله آزمایش ریخته 5 دقیقه به حالت سکون قرار میدهیم .با پی پت مایع رویی را خارج نموده 5 میلی لیتر آب اضافه نموده وهم زده مجددا 5 دقیقه به حالت سکون قرار داده سپس مایع رویی را خالی کرده وبه رسوب یک قطره بلودومتیلن اضافه کرده با پی پت پاستور از محتویات مقداری روی لام ریخته و لامل را روی لام قرار داده زیر میکروسکوپ با درشتنمایی 10x تخم فاسیولا،اورنیتو بیلارزیا،دیکروسلیوم را جستجو می کنیم .
توصیه های مهم
ü یکی دو ساعت قبل از آزمایش محلولها را خوب به هم می زنیم .
ü از تشکیل حباب هوا در لوله سانتریفوژ جلوگیری نماییم.
ü سرعت سانتریفیوژ را به تدریج زیاد نماییم.
چون تشخیص عفونتهای انگلی بستگی به یافته های تخم ،لارو،کیست،ترفوزوئیت و خود انگل در مدفوع دارد،مناسبترین روش جمع آوری و حمل نمونه ضروری می باشد.اگر نمونه ها کهنه ویا مقدار نا مناسب و همچنین بطور ناقص نگهداری شده باشد دارای ارزش کم وحتی منجر به تشخیص نا درست می گردد.
پس از جمع آوری باید از فیکساتورها و نگهدارنده ها استفاده گردد. Fixative برای حفظ شکل تک یاخته و پیشگیری از تغییر و تخریب نمونه می باشد.این مواد باید در حجمهای 30-15 میلی لیتر در ظروف پلاستیکی یا شیشه ای درب دار تهیه و درب آنرا محکم بسته تا از تراوش محتویات جلوگیری گردد. یک قسمت نمونه با سه قسمت فیکسا تیو تهیه نموده که باید در دمای 60 درجه سانتیگراد استفاده گردد.
انواع فیکساتورها و نگهدارنده ها
1-فرمالین 5% و 10 % برای نگهداری نمونه ( مدفوع ،تخم ،کرم ،لارو و کیست ) به نسبت 1 : 3
2- محلول نمکی فرمل 5 %برای نگهداری کیست ،تخم لارو جهت نگهداری طولانی مدت
طرز تهیه فرمالین 5 % : مقدار 5 میلی لیتر فرمالدئیدرا در 95 میلی لیترآب مقطرحل می نماییم .
طرز تهیه محلول نمکی فرمالین 5 % : 5 میلی لیتر فرم آلدئیدرا در 95 میلی لیتر سرم فیزیولوزی 0.85 % حل می نماییم.
از محلول لوگل بعنوان فیکساتیو و رنگ کننده میتوان استفاده نمود.
طرز تهیه محلول لوگل : 10 گرم (KI) + 5 گرم (I) + 100میلی لیتر آب مقطر
نکات مهم
1- در نماتودها از فرمالین بعنوان فیکساتیو نباید استفاده کرد.چون نفوذ آن تدریجی است و باعث سفتی و خشکی نمونه می شود. نماتودها را اول درآب گرم کشته و بعد سریعا به داخل نگهدارنده مناسب ( الکل-گلیسرین 5% )می گذاریم. اما از محلول 2-1 % فرمالین برای کشتن نماتودها میتوان استفاده نمود.
2-در ترماتودها بهترین فیکساتیو AFA (الکل- فرم آلدئید-اسید استیک ) می باشد که پس از 24 ساعت به محلول الکل گلیسرین 5 % باید منتقل نمود .
طرز تهیه AFA (الکل- فرم آلدئید-اسید استیک ) : 10میلی لیتر الکل اتیلیک 95 درجه + 5 میلی لیتر اسید استیک گلاسیال + 45 میلی لیتر آب مقطر
رنگ آمیزی کرمها به روش کارمن اسید
مواد مورد نیاز : 45 میلی لیتر اسید استیک + 55 میلی لیتر آب مقطر+ 5 گرم پودر رنگ
طرز تهیه رنگ کارمن : پودر رنگ را به اسید و آب مقطر اضافه نموده و مدت 15 دقیقه می جوشانیم.محلول را سرد کره وصاف می نماییم. مایع صاف شده بعنوان Stock استفاده می گردد.
روش رنگ آمیزی
1- انگل را حداقل بمدت 24 ساعت در ثابت کننده قرار می دهیم.
2- با آب معمولی نمونه را شسته تا ماده ثابت کننده خارج گردد.
3- بسته به ضخامت کرم نمونه را در رنگ کارمن اسید به مدت 6-2 ساعت قرار می دهیم.
4- نمونه را از رنگ خارج کرده و با آب بمدت 15 دقیقه شستشو می دهیم.
5- نمونه را در الکلهای 30-50و 70 درجه بمدت 60-30 دقیقه قرار می دهیم تا آبگیری شود.
6- نمونه را در اسید الکل 1 % قرار می دهیم تا رنگ اضافه خارج گردد.
7- نمونه را در الکل 70 درجه بمدت 3-2 ساعت قرار می دهیم .
8- در الکل 80 و سپس در الکل مطلق بمدت 1 ساعت قرار می دهیم.
9- نمونه را در مخلوط 50 % الکل اتیلیک مطلق و 50 % گزیلول بمدت 30 دقیقه قرار می دهیم
10- نمونه را در گزیلول خالص قرار می دهیم.
11- نمونه را با استفاده از کانادا بالزام مونته می نماییم(می چسبانیم).
روش نگهداری نمونه های مربوط به بند پایان
1) نگهداری مرطوب : برای نگهداری مرطوب از اتانول 80-70 درجه استفاده می گردد.
2) نگهداری خشک : برای معدوم کردن بندپا از اتر ،کلروفرم استفاده می گردد. پس از بی جان شدن، بوسیله سنجاق نازک آنرا به پایه هایی وصل نموده و سرانجام داخل جعبه ای قرار می دهیم،تا خشک شود.
روش شفاف سازی بند پایان
ابتدا بندپای مورد نظر یا قطعاتی از بدن آنرا از الکل خارج نموده و در یک لوله آزمایش محتوی پتاس 10-5 % به مدت 24 ساعت قرار می دهیم .میتوان لوله آزمایش حاوی نمونه و پتاس را در ظرفی که حاوی آب است قرار داده و به کمک حرارت آنرا جوشانید .این عمل برای کاهش زمان می باشد. بعد از شفاف شدن نمونه را در آب قرار داده تا پتاس اضافی ازآن خارج گردد.همچنین بقایای هیدرولیز شده نیز در این روش جدا می شود .سپس نمونه را در ظروف حاوی الکل با غلظتهای رو به افزایش ( 50-70-80-96 و الکل مطلق )قرار داده و سپس در مخلوط الکل –گزیلول به نسبت مساوی وارد نموده و سرانجام در گزیلول خالص قرار می دهیم.در نهایت نمونه را روی لام که ماده مانت کانادابالزام ریخته شده قرار داده و با یک لام تمیزآنرا می پوشانیم.
مواد و وسایل مورد نیاز : 1)الکل متیلیک مطلق 2)رنگ گیمسا 3)میکروسکوپ نوری 4)لام 5)روغن سدر
روش آزمایش
پس از تهیه گسترش از نمونه مدفوع آن را کنار گذاشته تا در مجاورت هوا خشک شود .با استفاده از متانول 96 درجه گسترش را Fix می کنیم .بعد از خشک شدن رنگ گیمسا ی غلیظ را به نسبت 1 به 20 با آب مقطر رقیق نموده و روی لام می ریزیم .بعد از 15 دقیقه (بسته به غلظت رنگ ) لام را شسته وبعد از خشک شدن یک قطره روغن سدر روی لام ریخته زیر میکروسکوپ با درشتنمایی ( ( 100xمشاهده می کنیم .
آزمایش نمونه مدفوع
آزمایش میکروسکوپی
1) آزمایش مستقیم : مقدار کمی از مدفوع تازه را برداشته بر روی یک لام با یک قطره سرم فیزیولوزی یا آب معمولی رقیق نموده و با قرار دادن یک عدد لامل بر روی آن در زیر میکروسکوپ مشاهده می نماییم. در آزمایش مستقیم مدفوع علاوه بر بررسی نمونه مدفوع ، آزمایش در یک قطره لوگل 5 % نیز ضروری می باشد .
2 ) روش رسوبی : در این روش حدود 10-5 گرم از مدفوع را در یک لیوان با 100 میلی لیتر سرم فیزیولوژی یا آب معمولی به خوبی مخلوط نموده واز یک توری عبور می دهیم.،تا آشغالهای آن در توری جمع گردد ولی تخم انگل و کیست انگلها از توری عبور کرده و در ظرفی زیر توری جمع گردد. محلول صاف شده را در یک لوله آزمایش ریخته و حدود نیم ساعت به حالت سکون قرار داده تا رسوب در ته لوله ایجاد گردد . پس از ته نشین شدن رسوب ، مایع رویی را خالی کرده و از رسوب آن با قطرات اضافی کنار لوله بصورت محلول در می آوریم.و یک قطره از آنرا برداشته روی لام قرار داده ویک عدد لامل روی آن گذاشته و زیر میکروسکوپ مشاهده می نماییم. آ
3)زمایش ریخته و حدود نیم ساعت ئ اااااا
روش مشاهده کریپتوسپوریدیوم و ایزوسپورابلی در مدفوع با استفاده از رنگ زیل- نلسون اصلاح شده :
1- گسترش را از نمونه تازه و یا فیکسه شده با فرمالین تهیه می نماییم.
2- گسترس را با متانول یا حرارت بمدت 5-2 دقیقه فیکسه می نماییم.
3- با کربول فوشین گسترش را بمدت 30-20 دقیقه رنگ امیزی می نماییم.
4- گسترش را باآب معمولی می شوییم.
5- به کمک اسید سولفوریک 5 % بمدت 60-20 ثانیه رنگ زدایی می کنیم.
6- گسترش را با آب معمولی می شوییم
7- به وسیله مالاشیت گرین ویا متیلن بلو(5 / 0%) بمدت 5 تا 4 دقیقه گسترش را رنگ می نماییم.
8- گسترش رنگ شده را شسته و در هوای آزمایشگاه خشک می نماییم.
اووسیست کریپتوسپوریدیم به رنگ قرمز در زمینه سبز یا آبی دیده می شود ،و در اووسیستها گرانول تیره رنگ مشاهده می شود.اسپوروبلاست در ایزوسپورابلی رنگ قرمز به خود می گیرد.
منبع:http://arm1354.blogfa.com
عقرب گزیدگی
از حدود 200 گونه متفاوت عقرب که د رسراسر دنیا پراکنده می باشند فقط حدود 20 گونه آنها سمی هستند در بین آنها گونه Mesobuthus Tamulus ( که نوعی عقرب قرمز هندی است) کشنده ترین گونه می باشد. که میزان کشندگی آن در ایالتهای هند بین 40-30 درصد گزارش شده است.
این جانور رنگهای مختلفی مثل زرد مایل به قهوه ای، قهوه ای، خاکستری و سیاه دارد و اندازه بین 18-5/1 سانتی متر دارد ولی بواسطه شکل بدنی خود که حالت تخت و صاف است،
می تواند از شکافهائی به عرض 3 میلی متر نیز عبور کند و خود را وارد خانه سازند.
در محیط خارج از خانه در شکاف و درز بین سنگها، زیر پوست درخت، بین هیزمها و ... یافت شده و در محیط داخل خانه حمام، دستشوئی، آشپزخانه و محیطهای مرطوب یافت می شوند. این جانوران در طول روز در گوشه ای بی حرکت و پنهان بوده و در طی شب فعالیت خود را آغاز می کنند و بدنبال شکار خود می روند و سم خود را از طریق نیش که در انتهای دم آنها وجود دارد به شکار خود تزریق می کنند.
· سم عقرب و علائم آن :
زهر اکثر عقربهای سمی باعث نابودی گلبولهای قرمز خون می شود و در محل گزش نیز تغییر رنگ موضعی و تورم دردناک ایجاد می کند، گر چه بطور متناقص سم بعضی از انواع کشنده مثلCentruroids باعث علائم موضعی و تورم زیاد نمی شود ولی حتماً باید توسط پزشک معاینه شده و با تزریق سرم ضد عقرب درمان شود، کودکان و افراد سالمند نیز نسبت به سم عقرب آسیب پذیرتر بوده و نیازمند توجه بیشتری می باشند .
علاوه بر آسیب به گلوبولهای قرمز، زهر عقرب علائم عصبی نیز ایجاد می کند که شامل:
بی قراری، تشنج، راه رفتن نامتعادل، تکلم منقطع، آبریزش از دهان، حساسیت شدید پوست به لمس، انقباضات ماهیچه ای، درد شکم و کاهش کارکرد سیستم تنفسی است.
البته در اکثر موارد این علائم در عرض 48 ساعت فروکش می کنند.
· درمان عقرب گزیدگی:
در اکثر موارد درمان عقرب گزیدگی مشتمل بر اقداماتی است که باعث تخفیف درد می شوند و فقط در مواردی که به گونه های خطرناک مشکوک می شویم ( توصیف بیمار از ظاهر عقرب و یا بدام افتادن عقرب توسط افراد دیگر و شناسائی گونه آن ) در صورت موجود بودن سرم عقرب از آن استفاده می کنیم. در هر صورت اقدامات زیر باید در مورد عقرب گزیدگی مد نظر قرار گیرد:
1. شستشوی محل زخم با آب و صابون و بیرون آوردن وسائل زینتی و جواهرات (مثل انگشتر و ... )
2. استفاده از کمپرس سرد برای کاهش درد و تورم
برای این کار می توان از یک تکه یخ استفاده کرد ولی هرگز نباید اندام گرفتار را در آب یخ غوطه ور ساخت.
3. برش محل زخم نیز فایده ای در بر ندارد و باید از آن پرهیز شود و همچنانکه استفاده از مکنده ( Suction ) نیز بی مورد است.
4. برای کاهش درد نیز از قرص استامینوفن ( 2-1 قرص هر 4 ساعت )می توان استفاده کرد ولی از آسپرین و ایبوبروفن باید پرهیز شود.
5. آنتی بیوتیک نیز کمک کننده نمی باشد.
6. فرد عقرب گزیده باید به آرامش و خونسردی دعوت شده و اضطراب را از وی دور کرد.
7. فرد مصدوم به هیچ وجه در طول مدتی که تحت نظر است نباید از مشروبات الکلی و یا داروهائی که فرد را گیج می کند ( مثل انواع خواب آورها) استفاده کند.
8. در صورت امکان عقرب مسوؤل گزش فرد، باید بدام انداخته شود تا گونه آن مشخص گردد.
9. تمام افراد عقرب گزیده حتی خفیف ترین انواع آن باید حداقل 24 ساعت در بیمارستان تحت نظر باشند.
· اقدامات پیشگیرانه برای کنترل عقرب در محیط زندگی:
1- هیزم ، الوار ، سنگ و هر گونه زباله از مجاورت محل زندگی باید زدوده شود.
2- در هنگام تمیز کردن این مکانها باید از دستکش و وسائل حفاظتی دیگر استفاده کرد.
3- درز درها و پنچره ها و هرگونه شکافی در ساختمان باید مسدود شده تا از ورود عقرب به داخل خانه جلوگیری شود.
4- در آب و هوای خشک استفاده از کیسه و یا گونی های کرباسی خیس در اطراف خانه باعث بدام افتادن عقربها می شوند.
5- استفاده از آفت کشها و حشره کشها که با نابود کردن جاندارانی که غذای عقرب محسوب می شوند. می تواند بصورت غیرمستقیم باعث کاهش تعداد عقربها در محل زندگی شود.
6- استفاده از مواد شیمیائی عقرب کش نیز مستقیماً باعث نابود کردن عقربها
می شود.
منبع:http://www.bpums.ac.ir
حقیقتی راجع مارها

افعی سبز جنگلی
- مارهایی که در دریا زندگی می کنند دارای آبشش نیستند و برای تنفس مجبور هستند که به سطح آب بیایند. اما با این حال توانایی آنرا دارند که ساعتها زیر آب بدون آنکه روی سطح آب بیایند، بمانند. آنها توانایی آنرا دارند که در این مدت از اکسیژن محلول در آب استفاده کنند.
- تاکنون حدود 2500 گونه مار شناسایی شده است که از این میان فقط 20 درصد از آنها سمی هستند.
- یک مار بزرگ پیتون می تواند یک موجود زنده به وزن 70 کیلوگرم را به راحتی ببلعد، اما هضم این لقمه ممکن است برای او بسیار دشوار باشد.
- مارها دارای حس بویایی بسیار قوی هستند و از آن برای جستجو و شکار استفاده می کنند. علاوه بر این برخی از انواع مارها با تشخیص حرارت بدن طعمه، آنرا ردیابی و شکار می کنند.
- بسیاری از گونه های مار از جمله مار کبری از طریق ارتعاشات هوا نمی توانند چیزی بشنوند. برعکس آنها لرزش ناشی از حرکت یا صوت را از طریق بدن خود که روی زمین می باشد احساس می کنند.
- مارها توانای حرکت با سرعت بالا را ندارند. بیشترین سرعتی که برای حرکت مارها ثبت شده است حدود 13 کیلومتر بر ساعت می باشد.
- بیشترین طول عمری که برای یک مار مشاهده شده است کمتر از 30 سال می باشد که مربوط به نوع آناکوندا (Anaconda) و مار کبرای سیاه می باشد.
- سم مامبای سیاه (Black Mamba) باعت مختل شدن سریع اعصاب می شود و از قویترین سموم شناخته شده مارها می باشد. برای همین اغلب پاد زهر های سم مار را از آن می سازند.
- مارها به دلیل کوچک بودن بخشی از مغزشان که وظیفه یادگیری را بعهده دارد هرگز توانایی یاد گیری ندارند.
- اغلب مارها حدود 200 دندان دارند که از آن برای نگهداری از طعمه خود استفاده می کنند. آنها بهیچ وجه به کمک این دندانها نمی توانند طعمه را بجوند چرا که این دندانها به سمت عقب متمایل می باشند، اما با آنها گاز میگیرند.
منبع:http://kashef.ropage.com
كپكی كه سبب كشف پنی سیلین شد

شاید معروفترین اكتشاف تصادفی مهم، كشف پنی سیلین به دست سر الكساندر فلمینگ باشد. اما در این اكتشاف، بیش از آنچه اكثر افراد تصور می كنند، بخت یاری دخالت داشته است؛ گر چه كشف فلمینگ پیامدهای شگفت آوری داشت كه بدان اهمیت بخشیدند، اما این پیامدها كمتر شناخته شده اند.
زندگی فلمینگ مملو از وقایع به ظاهر نامربوطی است كه در عین حال اگر حتی یكی از آنها هم روی نمی داد، چه بسا فلمینگ به شهرتی كه بدان دست یافت نمی رسید. همان گونه كه دوست و همكارش پروفسورس.آ. پانت به هنگام مرگش در ستایش او گفت: شخص احساس می كند نمی تواند آنها را ناشی از تصادف محض بداند .
الكساندر فلمینگ در سال 1881 در روستای آیرشایراسكاتلند به دنیا آمد. وقتی هفت ساله بود پدرش درگذشت و مسئولیت اداره مزرعه و تربیت چهار فرزند تنی و چند فرزند ناتنی به دوش مادر الكساندر افتاد. وقتی الكساندر پنج ساله بود، پیاده به مدرسه ای در 5/1 كیلومتری می رفت و وقتی دهساله شد، مجبور بود فاصله 5/6 كیلومتری خانه تا مدرسه را پیاده طی كند. هنگامی كه به دوازده سالگی رسید مدرسه اش بیش از 25 كیلومتر با خانه فاصله داشت، بنابراین در آكادمی كیلمارناك اقامت گزید. با این حال مجبور بود در تعطیلات آخر هفته حدود 20 كیلومتر راه رفت و برگشت از ایستگاه قطار تا منزل را طی كند. پس از یك سال و نیم اقامت در كیلمارناك به لندن پیش برادرش رفت و تحصیلات خود را در پلی تكنیك ادامه داد. اما این دوران دیری نپایید، چون الكساندر توان مالی تحصیل در آنجا را نداشت. فلمینگ شانزده ساله در یك شركت كشتیرانی استخدام شد و كمی از وقت خود را با نیروهای داوطلب اسكاتلندی مقیم لندن گذراند. او در تیم واترپولوی این گروه بازی می كرد، و یك بار با تیمی از بیمارستان سن مری، وابسته به دانشگاه لندن، مسابقه داد.
چند سال بعد ارث مختصری به او رسید و برادرش او را تشویق كرد تا وارد دانشكده پزشكی شود. در لندن دوازده دانشكده پزشكی بود، كه فلمینگ از هیچ كدامشان شناختی نداشت- جز یكی كه بیمارستان سن مری وابسته به آن بود و تنها چیزی كه می دانست این بود كه یك تیم واترپولو دارد، و به همین دلیل به آنجا رفت. در همان هنگام بود كه المرات رایت به عنوان مدرس باكتری شناسی در آن دانشكده مشغول به كار شد. فلمینگ در ابتدا تصمیم داشت جراح شود، اما پس از فارغ التحصیلی، شغلی در آزمایشگاهی كه در آن موقع المرات رایت سرپرستی آن را به عهده داشت به او پیشنهاد شد؛ فلمینگ تا پایان عمر خود را در آن آزمایشگاه گذراند و در سال 1929 استاد باكتری شناسی شد.
طی جنگ جهانی اول فلمینگ و رایت به فرانسه اعزام شدند تا به معالجه سربازان زخمی بپردازند. آن زمان پزشكان برای درمان جراحت های جنگی از مواد ضد عفونی كننده استفاده می كردند. اما فلمینگ متوجه شد كه فنل ( یا اسید كربولیك كه رایجترین ماده ضد عفونی كننده آن زمان بود) بیشتر ضرر دارد تا فایده، چون گویچه های سفید خون را سریع تر از باكتری ها نابود می كند. فلمینگ می دانست كه این اثر زیانمند است چون گویچه های سفید ، مدافعان طبیعی بدن در برابر باكتری ها هستند.
در سال 1922فلمینگ برحسب تصادف میكروب كشی كشف كرد كه باكتری ها را از بین می برد، اما بر گویچه های سفید اثری نمی گذاشت. هنگامی كه فلمینگ دچار زكام شد، از ترشحات بینی خود كشتی تهیه كرد. همچنان كه ظرف كشت را كه پر از باكتری های زرد رنگ بود بررسی كرد، اشكی از چشمش به درون ظرف افتاد. روز بعد وقتی كشت را مورد مطالعه قرار داد، در قسمتی كه اشك ریخته بود فضای شفافی دید. كنجكاوی و تیزبینی اش او را به نتیجه صحیح راهنمایی كرد. در اشك ماده ای بود كه باعث تخریب سریع ( لیز) باكتری ها می شد، اما به بافت انسان آسیبی نمی رساند. او این آنزیم ضد میكروبی اشك را لیزوزیم نامید. معلوم شد كه این آنزیم اهمیت كاربردی چندانی ندارد، چون میكروب هایی كه لیزوزیم از بین می برد نسبتاً بی ضرر هستند، اما چنان كه خواهیم دید، این اكتشاف مقدمه ضروری كشف پنی سیلین بود.
در تابستان سال 1928 فلمینگ مشغول تحقیق درباره آنفلوانزا بود. ضمن انجام كارهای معمول آزمایشگاهی كه می بایست كشت های باكتریایی را كه در ظرفهای پهن در پوش دار رشد كرده بودند زیر میكروسكوپ بررسی كند، متوجه شد كه در یكی از ظرف ها ناحیه شفافی به وجود آمده است. تحقیقات بیشتر نشان داد كه ناحیه شفاف در اطراف نقطه ای بود كه ظاهراً وقتی سرپوش ظرف گذاشته نشده بود، تكه ای كپك به درون آن افتاده بود. فلمینگ با به خاطر آوردن تجربیاتش در زمینه لیزوزیم، نتیجه گرفت كه كپك چیزی تولید می كرد كه باعث مرگ باكتری های استافیلوكوك در ظرف كشت شده بود. فلمینگ تعریف كرد:
اگر تجربیات قبلی ام نبود[ درباره لیزوزیم] چه بسا مانند كاری كه بسیاری از باكتری شناسان دیگر قبلاً كرده بودند ظرف را به دور می انداختم. به احتمال زیاد برخی از باكتری شناسان هم متوجه تغییراتی مشابه آنچه من دیدم شده بودم، اما چون علاقه ای به مواد ضد باكتریایی طبیعی وجود نداشت، كشتها را به دور اندخته بودند. من به جای آنكه مطابق رسم زمانه كشتهای آلوده را دور بیندازم، تحقیقاتی انجام دادم.
فلمینگ كپك را جدا كرد و آن را به عنوان یكی از اعضای جنس پنی سیلیوم شناخت، و ماده آنتی بیوتیكی را كه تولید می كرد پنی سیلین نامید. بعدها گفت: هزاران كپك مختلف وجود دارد و هزاران باكتری مختلف، و این كه بخت ، كپك را در لحظه مناسب در نقطه مناسب بگذارد مثل برنده شدن در مسابقه بخت آزمایی بود. ذكر هزاران باكتری مختلف آن قدر هم بی مورد نبود، چون گرچه پنی سیلین برای باكتریهای متعددی، ازجمله استافیلوكوك، مرگبار است، اما بر برخی از انواع دیگر باكتری ها اثری ندارد. خوشبختانه باكتری هایی كه پنی سیلین از بین می برد، سبب بسیاری از عفونت های شایع و خطرناك در انسان هستند.
البته در سال 1928 استفاده از كپك برای مقابله با عفونت ، ابتكار كاملاً نوظهوری نبود. لویی پاستور و همكارش ژ. ف. ژوبر در سال 1877 نشان داده بودند كه گاه میكروبی از رشد میكروبی دیگر جلوگیری می كند. نوشته اند كه درعهد باستان مصریان و رومیان از كپك نان استفاده می كردند، اما هزاران كپك مختلف بر نان می رویند كه تنها چند نوع آنها چیزی تولید می كنند كه با عفونت مقابله كند. قاعدتاً فلمینگ هم از این مسئله مطلع بود و به همین سبب در می یابیم كه چرا شگفت زده شد.
فلمینگ در ادامه نشان داد كه پنی سیلین برای جانوران سمی نیست و به یاخته های بدن آسیبی نمی رساند:
همین سمی نبودن پنی سیلین برای گویچه های سفید بود كه باعث شد متقاعد شوم روزی به عنوان ماده ای دارویی شناخته خواهد شد. وقتی پنی سیلین خام در خون انسان آزمایش می شد، رشد استافیلوكوكها را در رقت 1 در 1000 كاملاً مهار كرد، اما اثر سمی آن بر گویچه های سفید چیزی بیش از محیط كشت اولیه نبود. آن را به جانوران نیز تزریق كردم، و ظاهراً هیچ اثر سمی نداشت. چند آزمایش ابتدایی [ بربیماران] نتایج مطلوبی داد اما اتفاق معجزه آسایی نیفتاد، و فهمیدم كه باید آن را غلیظ می كردیم . سعی می كنیم پنی سیلین را تغلیظ كنیم اما دریافتیم كه پنی سیلین به سرعت خراب می شود، و روشهای نسبتاً ساده ما فایده ای نداشتند.
در همین هنگام موفقیت چشمگیر سولفانیل آمید باعث شده بود كه شیمی درمانی توجه همگان را به خود جلب كند . همكاری هرولد ریستریك و فلمینگ برای جدا سازی و تغلیظ پنی سیلین با شكست مواجه شد، و تا چندین سال بعد دیگر كار مهمی درباره پنی سیلین انجام نگرفت. در اواخر دهه 1930 هاوارد و. فلوری استاد آسیب شناسی دانشگاه آكسفورد همكاری پژوهشی خود را با ارنست بوریس چین ، زیست شیمیدان پناهنده یهودی كه از آلمان هیتلری گریخته بود و به سفارش فلوری به آكسفورد آمده بود، آغاز كرد. آن دو تحقیق درباره لیزوزیم، همان آنزیم ضد باكتریایی كه فلمینگ كشف كرده بود، و نیز دیگر مواد ضد باكتریایی طبیعی را شروع كردند. چندی نگذشت كه پژوهش های آنان بر پنی سیلین كه به نظر آنان امید بخش ترین این عوامل بود متمركز شد.
گروه آكسفورد با بهره گیری از روشهای پیچیده شیمیایی برای جداسازی و تغلیظ، كه امكانات آن در آكسفورد وجود داشت و فلوری و چین با آن آشنا بودند، اما فلمینگ در سن مری نه با آنها آشنایی داشت و نه بدانها دسترسی، موفق شدند پنی سیلین را آن قدر تغلیظ و تصفیه كنند كه خواص درمانی آن را ابتدا در مقابله با عفونت های تجربی در موش و بعداً در افراد بیماری كه از عفونت های استافیلوكوكی و دیگر آلودگی های خطرناك رنج می بردند، به اثبات رسانند ( نخستین پنی سیلین را كه در انسان استفاده می شد، در لگن های بیمارستانی رشد می دادند؛ با آنكه پنی سیلین را از ادرار بیماران جدا می كردند و مجدداً مورد استفاده قرار می دادند، اما برخی آزمایش های بالینی به دلیل كمیاب بودن این دارو ناتمام ماندند).
به سبب ضرورت بهره گیری سریع از توانایی پنی سیلین در مقابله با بیماری ها و درمان زخمهای نظامیان جنگ جهانی دوم، تولید آن در مقیاس گسترده، هم در انگلستان و هم در ایالات متحده، از اولویت های اول بود. فلوری به آمریكا رفت تا روشهای استخراج و تولید پنی سیلین در انگلستان را شرح دهد، و شیمیدانان دو سوی اقیانوس اطلس به طور خستگی ناپذیری كار كردند تا ساختار شیمیایی پنی سیلین را تعیین كنند و از راه تخمیر یا تولید آزمایشگاهی آن را به دست آورند. این مولكول پیچیده و ناپایدار برای نخستین بار سالها پس از پایان جنگ به طور صناعی تهیه شد، اما پیشرفت در گسترش تولید آن از راه تخمیر در مدت جنگ به نحوی استثنایی سریع بود.
همان طور كه بخت یاری در كشف پنی سیلین نقش داشت، در این مرحله از تولید آن نیز وارد صحنه شد. وقتی فلوری به ایالات متحده رفت تا درباره تولید پنی سیلین در مقیاس وسیع تبادل نظر كند، از آزمایشگاه پژوهشی ناحیه شمال وابسته به وزارت كشاورزی ایالات متحده در پئوریای ایلینویز دیدن كرد. مدتی بود كه در این آزمایشگاه به دنبال كاربردی صنعتی برای محصول غلّه اضافی، و راه حلی برای مشكلی كه در همین رابطه وجود داشت، یعنی دفع ماده چسبناكی كه به عنوان یكی از فراورده های جانبی از فرایند آسیاب كردن ذرت به دست می آمد، جست و جو می كردند. وقتی این ماده استخراج شده به محیط كشت پنی سیلین اضافه شد، بازدهی كپك مورد نظر را به طور نامنتظره ای ده برابر افزایش داد.
دومین كمكی كه آزمایشگاه پئوریا كرد تهیه سویه بهتری از كپك مولّد پنی سیلین بود. صدها كپك از سرتاسر جهان جمع آوری و برای آزمایش به پئوریا فرستاده شدند. شگفت آنكه بهترین كپك را یكی از زنان محلی به نام مری هانت فرستاد، كه به دلیل علاقه اش به جست و جو برای كپك های جدید، مری كپكی لقب گرفته بود. او از یكی از بازارهای میوه پئوریا یك طالبی آورد كه كپكی با ظاهری قشنگ و طلایی روی آن بود. این سویه جدید كپك بازدهی پنی سیلین را دو برابر كرد، بنابراین تركیب دو اكتشافی كه در پئوریا صورت گرفت میزان بازدهی پنی سیلین را به 20 برابر رساند. چه كسی فكر می كرد پئوریا این قدر در تولید داروی معجزه آسایی كه برحسب تصادف در لندن كشف شده بود، نقش پیدا كند؟
استفاده از پنی سیلین نه تنها جان هزاران نفر را طی جنگ جهانی نجات داد، بلكه عاملی شد تا برای كشف آنتی بیوتیك های دیگر، از جمله خانواده ای از تركیبات مشابه شیمیایی پنی سیلین به نام سفالوسپورینها، پژوهش هایی انجام گیرد. برخی از این آنتی بیوتیك های جدید در مبارزه با باكتری هایی كه به پنی سیلین مقاوم اند مؤثر هستند .
فلمینگ، فلوری و چین جایزه نوبل در فیزیولوژی یا پزشكی را در سال 1945 مشتركاً بردند. هر سه متعاقباً به سبب پژوهشهایشان، كه منجر به تسكین آلام و نجات جانهای بی شماری شده بود، به لقب سر نایل شدند.
سِرالكساندر فلمینگ به بهره ای كه از بخت یاری برد، آگاه بود. یك بار گفت: سرگذشت پنی سیلین جنبه عاطفی خاصی دارد و نشان می دهد كه چقدر بخت، اقبال، سرنوشت، تقدیر، یاهر چیزی كه اسمش را می گذارید، در زندگی هر كس نقش دارد . باید اضافه كنم كه اگر هوشمندی یا – اگر بخواهیم جزء اساسی تعریف والپول از بخت یاری را به كار ببریم – ذكاوت فلمینگ نبود، تصادف هایی كه برایش اتفاق افتادند به هیچ چیزی نمی انجامیدند.
منبع:http://www.tebyan.net
داستان كشف باكتری كـُش ها
كشف سولفانیل آمید و داروهای باكتری كش صناعیِ شبیه به آن ، به همان اندازه كه از بخت یاری ناشی شد، نتیجه یك اشتباه بود. "گرهارد دوماگ" جایزه نوبل فیزیولوژی یا پزشكی را در سال 1939 به سبب كشف آن دریافت كرد، اما بسیاری دیگر نیز نقش های مهمی در این قضیه داشتند.
دوماگ در سال 1895 در لاگو آلمان به دنیا آمد. وارد دانشگاه كیل شد، اما جنگ جهانی اول در تحصیلات پزشكی او فاصله انداخت. او پس از امضای قرارداد متاركه جنگ به دانشگاه كیل بازگشت، و در سال 1921 دانشنامه پزشكی اش را دریافت كرد. پس از چند سال تدریس در دانشگاه گریفسوالد و استادی در انستیتو آسیب شناسی مونستر، در سال 1932 در مجتمع صنعتی آی جی فاربن كه كارتل آلمانی بازار رنگ بود، به عنوان سرپرست آزمایشگاه باكتری شناسی و آسیب شناسی تجربی آن مشغول به كار شد. در آنجا وظیفه اش آزمایش بر روی خواص دارو شناختی رنگهای جدیدی بود كه "فریتز میتسش" و "ژوزف كلارر" شیمیدان تهیه می كردند. میتسش با تهیه نخستین داروی موفق ضد مالاریایی صناعی به نام آتابرین به شهرت رسیده بود. مالاریا عفونتی تك یاخته ای نظیر سیفیلیس است كه ارلیش ، داروی سالوارسان را علیه آن مؤثر یافته بود- این نخستین تیر جادویی بود كه از راه شیمی درمانی علیه بیماری استفاده شد. اما در سال 1932 هیچ ماده شیمیایی علیه باكتری ها مؤثر نبود- همان باكتری هایی كه بیماری های مخوفی همچون ذات الریه، مننژیت، سوزاك، و عفونت های استرپتوكوكی و استافیلوكوكی را ایجاد می كنند.
گروه شیمیدانان و داروشناسان "آی جی فاربن" تصمیم گرفتند تركیباتی بیابند كه این میكروب ها را نابود كنند، بی آنكه به جانوران یا انسان های میزبانشان آسیبی برسانند. نقشه ای كه طرح ریزی كردند این بود كه رنگهای بخصوصی تهیه كنند، و تعیین كنند آیا امكان دارد باكتری كش باشند یا نه . چون به نظر می رسید برخی از انواع رنگ ها بویژه آنهایی كه در آنها یك گروه سولفونامید بود در پارچه های پشمی بسیار پایدار باشند، و همین نشان می داد كه تمایل زیادی برای اتصال به مولكول های پروتئین دارند. شیمیدانان گمان كردند كه شاید چون باكتری ها پروتئینی هستند این رنگها خود را به باكتری ها بچسبانند و آنها را مهار یا نابود كنند. همان طور كه خواهیم دید این نظریه فقط تا حدی درست بود: وجود گروه سولفونامید ضروری بود، اما قسمتی از مولكول كه به آن خواص رنگی می داد نقشی در خاصیت باكتری كشی نداشت.
یكی از رنگ هایی كه میتسش و كلارر تهیه كردند و دوماگ روی خرگوش ها و موش های آزمایشگاهی آلوده به استرپتوكوك امتحان كرد، پرونتوسیل نام داشت. معلوم شد كه این ماده در زدودن این باكتری ها بسیار مؤثر است، و جانوران مقادیر زیاد آن را بدون هیچ عارضه ناگواری تحمل می كنند. كشف این اثر باكتری كشی در جانوران احتمالاً در اوایل سال 1932 صورت گرفت؛ آی جی فاربن متعاقباً در دسامبر همان سال تقاضا كرد آن را به نام شركت ثبت كنند. ظاهراً آزمایش های بالینی در افراد بیمار ، كمی پس از آن شروع شد، اما روایت های گوناگونی وجود دارد. برخی می گویند قبل از آنكه هرگونه آزمایشی در انسان صورت گیرد، دوماگ از روی ناچاری مقداری پرونتوسیل به دختر بیمار و در حال مرگ خود كه به دنبال زخم سوزنی دچار عفونت استرپتوكوكی خطرناكی شده بود داد و دختر به سرعت بهبود یافت. دیگران نقل می كنند كه نخستین آزمایش بالینی بر روی پسر بچه ده ماهه ای انجام گرفت كه براثر آلودگی خونش به استافیلوكوك رو به مرگ بود. پزشك معالجش "ریشارد فورستر" به او پرونتوسیل داد. فورستر دستیار دكتر "هانس شروس" بود، كه در دانشكده پزشكی دوسلدروف مقام استادی داشت و از دوستان "هاینریش هورلین" بود، كه در آی جی فاربن مافوق دوماگ بود. وقتی فورستر درباره پسربچه مریض از شروس مشورت خواست، شروس به یاد آورد كه هورلین درباره رنگ قرمزی ( پرونتوسیل ) با او صحبت كرده بود كه به طور معجزه آسایی در جانوران برای مقابله با استرپتوكوك مؤثر بود. چون كودك در هر صورت به مرگ نزدیك شده بود، فورستر احساس كرد كه اگر هم رنگ در مقابله با استافیلوكوك مؤثر نباشد چیزی را از دست نمی دهد، بنابراین دوبار رنگ قرمز را به كودك داد، و بیماری كودك كه تصور می شد مسمومیت مهلك خون باشد، به سرعت درمان شد. حال كدام یك از این دو سرگذشت درست است، یا اصولاً صحت دارند یا نه، فرقی نمی كند، اما همین قدر مسلم است كه تا اواسط دهه 1930 آوازه این معجزه پزشكی به همگان رسیده بود، و برهمین اساس جایزه نوبل سال 1939 به دوماگ اعطا شد.
اما پیشرفت های مهم دیگری نیز در سال های 1933 تا1939 صورت گرفت. دوماگ تا فوریه سال 1935 یعنی بیش از دو سال پس از انجام آزمایش ها و یك ماه پس از ثبت پرونتوسیل به نام آی جی فاربن، نتایجی را كه از آزمایش پرونتوسیل در عفونت های جانوری به دست آورده بود منتشر نكرد. زن و شوهری در انستیتو پاستور پاریس به نام ژ. وژ. ترفوئل زیر نظر م. فورنو از پژوهش های آلمانی ها مطلع شدند و كشف بنیادینی كردند. آنان چندین تركیب را كه از لحاظ ساختار شیمیایی شباهت زیادی به پرونتوسیل داشتند و رنگ های " آزو" خوانده می شدند بررسی كردند. واژه آزو كه به این رنگ بخصوص اطلاق می شود مشتق از معادل فرانسوی نیتروژن یا ازت است، و بدین دلیل استفاده می شود كه در وسط مولكول دو اتم نیتروژن با پیوند دوگانه به یكدیگر متصل شده اند. این رنگها در یك قسمت مولكول تفاوت عمده ای با پرونتوسیل دارند، اماهمه آنها دارای بخش سولفونامید هستند. ترفوئلها دریافتند كه خواص ضد باكتریایی این رنگ ها تقریباً تفاوتی با پرونتوسیل ندارد.
این یافته همچنین معمای دیگری را درباره پرونتوسیل توضیح می داد: این كه چرا در لوله آزمایش در مقابله با باكتری ها اثری نداشت در حالی كه در بدن جانداران بسیار مؤثر بود؟ به دیگر سخن، یكی از فعالیت های بدن باعث می شد رنگهای سولفونامید اثر ضد باكتریایی پیدا كنند. دانشمندان فرانسوی استدلال كردند كه در بدن جانور، رنگ به دو قسمت شكسته می شود، و تنها نیمه سولفونامید است كه عامل ضد باكتریایی مؤثری است. آنان برای اثبات این مطلب از پرونتوسیل ، بخش ساده تر آن را یعنی سولفونامید كه به تركیب پ – آمینوبنزن سولفونامید معروف بود و به اختصار" سولفانیل آمید" خوانده می شد تهیه كردند، و دریافتند كه در مقابله با عفونت های باكتریایی به اندازه پرونتوسیل مؤثر است. فرمول های پرونتوسیل و سولفانیل آمید در شكل 1 نمایش داده شده اند. اگر مولكول پرونتوسیل در محل پیوند دو گانه بین اتمهای نیتروژن میانی ( قسمتی كه با پیكان نشان داده شده است) شكسته شود و دو اتم هیدروژن به قسمت سمت راست اضافه شود، سولفانیل آمید به دست می آید. وقتی پرونتوسیل به جانور تزریق یا خورانده شود، در بدن می شكند، و سولفانیل آمیدی كه بدین ترتیب ایجاد می شود عامل ضد باكتریایی اصلی است. سولفانیل آمید مانند نیمه دیگر مولكول پرونتوسیل بی رنگ است، اما پیوند این دو قسمت از راه پیوند دو گانه بین دو اتم نیتروژن مركزی رنگ آزو را رنگین می كند. این نظریه كه رنگ های سولفونامید باكتری كش باشند تصوری اشتباه بود چون تنها بخش سولفونامید مولكول رنگ است كه خاصیت میكروب كشی دارد؛ و این كه سولفونامید جزئی از مولكول رنگ را تشكیل می داد امری تصادفی بود، و به همین سبب است كه باید این اكتشاف را بخت یارانه دانست.
كشف ترفوئل ها حق امتیاز پرونتوسیل را كه در اختیار آی جی فاربن بود بی فایده ساخت. گر چه سولفانیل آمید سال ها قبل به عنوان ماده رنگی واسطی تهیه و به ثبت رسیده بود، اما تا وقتی معلوم شد كه این ماده باكتری كش نیرومندی است، امتیاز آن منقضی شده بود.
به دنبال اعلام یافته های فورنو از انستیتو پاستور در سال 1935، آزمایشهای بالینی سولفانیل آمید در فرانسه، انگلستان و ایالات متحده با موفقیت معجزه آسایی رو به رو شد. از مواردی كه توجه بسیاری را به خود جلب كرد استفاده از پرونتوسیل در نجات جان فرانكلین د. روزولت كوچك، فرزند رئیس جمهور امریكا بود. در سال 1936 روزولت نوجوان براثر عفونت استرپتوكوكی رو به مرگ بود، كه به درخواست مادرش النور روزولت، دكتر جورج توبی در بیمارستان عمومی ماساچوست به او پرونتوسیل داد و بیمار به سرعت بهبود یافت.
شیمیدانان، بسیاری از مواد ساده مشابه سولفانیل آمید را تهیه، و روی جانوران و سپس انسان ها آزمایش كردند؛ در واقع تا سال 1947 بیش از 5000 سولفونامید شبیه سولفانیل آمید تهیه و آزمایش شده بودند. همه اینها مؤثر نبودند، اما معلوم شد كه بعضی در مقابله با بیماری های خاصی مؤثرتر از سولفانیل آمید هستند. مثلاً سولفاپیریدین در سال 1938 به دست آمد و مشخص شد كه در مقابله با ذات الریه مؤثرتر است، و سولفاتیازول نیز در سال 1940 تولید شد و مصرف پزشكی پیدا كرد.
پسنوشت
ساختار مولكولی سولفونامیدهای مؤثر به نحو چشمگیری به یكدیگر شبیه است. از هزاران تركیبی كه تهیه و آزمایش شده اند تقریباً در تمام موارد، آنهایی فعال اند كه تنها اختلاف ساختاری آنها در گروه اتمهای متصل به سمت راست اتم نیتروژن پررنگی باشد كه در شكل 2 در فرمول های سولفا پیرندین و سولفاتیازول مشخص شده است.داروهای سولفا در دهه 1940 با موفقیت بسیاری بویژه برای مداوای نیروهای مسلح در جنگ جهانی دوم استفاده شدند. بعدها پنی سیلین و دیگر آنتی بیوتیك های امروزی تا حد زیادی جانشین آنها شدند، اما با وجود این هنوز هم در درمان برخی از بیماری ها مورد استفاده اند. یكی از معایب آنها نامحلول بودنشان بود كه منجر به رسوب در كلیه ها و آسیب زدن به آنها می شد. معلوم شد كه می توان با تجویز تركیبی از سه داروی سولفای مختلف این مشكل را تخفیف داد، به نحوی كه مجموع مقداریشان به اندازه مقداری مساوی از یكی از آنها اثر داشته باشد، اما غلظت هر كدام یك سوم مقدار معمول باشد تا به طور مطلوب دفع شود.
گفتیم كه دوماگ جایزه نوبل سال 1939 را دریافت كرد. اما این گفته كاملاً درست نیست. گرچه مقامات استكهلم او را برای اعطای جایزه برگزیدند، اما در واقع او تا چندین سال بعد آن را دریافت نكرد. وقتی خبر انتخاب دوماگ در اكتبر سال 1939 به دستش رسید، نامه ای مبنی بر پذیرش آن فرستاد، اما در نوامبرنامه دومی به استكهلم رسید كه در آن جایزه را رد كرده بود. نامه دوم در نتیجه ی فشار نازی ها نوشته شد، چون در آن هنگام دوماگ در چنگ گشتاپو بود. پس از جنگ، دوماگ توانست در سال 1947 به استكهلم برود، سخنرانی مراسم اعطای جوایز را ایراد كند و نشان و لوح افتخاری دریافت دارد – اما از پول جایزه نصیبی نبرد، چون به صندوق بنیاد نوبل عودت داده شده بود.
منبع:http://www.tebyan.net
خرس قطبی چگونه جانوری است؟

خرس قطبی فقط در قطب شمال زندگی می كند و بیشتر عمرش را روی یخهای شناور می گذراند. این حیوان بزرگترین جانور گوشتخوار خشكی و بزرگترین عضو خانواده خرسهاست و با سرمای اقیانوس منجمد شمالی به خوبی سازگار شده است. این حیوان بین 4 تا 8 سالگی بالغ و آماده تولید مثل می شود و هر بار یك تا سه توله به دنیا می آورد و 25 تا 30 سال عمر می كند.
غذای خرس را بیشتر ، خوكهای دریایی تشكیل می دهند. اما گاهی پستانداران دیگر، تخم پرندگان، لاشه های افتاده بر ساحل و سبزیها را نیز می خورد. بویایی خرس قطبی بسیار قوی است به طوری كه می تواند بوی لاشه نهنگ یا خوك مرده را از 30 كیلومتری احساس كند.
رنگ خرس قطبی ، سفید شیری است و بینی و دهان و چشمانش سیاه هستند. در یك روز آفتابی با یك دوربین معمولی از فاصله 10 كیلومتری می توان بینی او را دید و اگر او را در جایی غیر از قطب نگهداری كنند، رنگ موهایش كم كم خاكستری می شود.

خرس قطبی نرِ بالغ حدود 260 سانتیمتر قد و 450 كیلوگرم وزن، و ماده آن حدود دو متر قد و 250 كیلوگرم وزن دارد. جالب این است كه توله ی او هنگام تولد چندان بزرگتر از یك موش صحرایی نیست و فقط حدود نیم كیلوگرم وزن دارد. توله های خرس قطبی دندان ندارند و پوستشان بدون مو است و به مراقبت مداوم مادرشان نیازمندند. آنها پس از سه ماه كه برای نخستین بار از لانه شان بیرون می آیند حدود 13 كیلوگرم وزن پیدا كرده اند. شیر خرس قطبی 9 برابر از شیر گاو چربتر است و سبب رشد سریع توله ها می شود.
خرس قطبی شناگر ماهری است و می تواند با سرعت 10 كیلومتر در ساعت شنا كند. موهای میان تهی خرس قطبی او را در شنا كردن و همین طور در برابر سرمای قطب كمك می كند. خرس قطبی در شكار خوك آبی مهارت خاصی دارد. او می گردد و سوراخی را كه خوك برای رفتن به داخل آب روی یخ ایجاد كرده پیدا می كند و بعد با حوصله منتظر می ماند تا خوك برای نفس كشیدن به سوراخ برگردد . در این موقع به راحتی او را شكار می كند. لازم به ذكر است كه بومیان قطب شمال از پوست و گوشت خرس قطبی استفاده می كنند.
منبع:http://www.tebyan.ne
آیا می دانید ادوارد جنر چگونه موفق به كشف واكسن آبله شد ؟
مطابق مقاله ای كه ا.ل. كامپیر در سال 1957 تحت عنوان پژوهش، بخت یاری و جراحی ارتوپدی نوشت كه شهرت ادوارد جنر به دلیل آشنا كردن جهانیان با واكسنی است كه جان میلیونها نفر را از مرگ شوم ناشی از آبله رهانیده و چندین میلیون نفر دیگر را از ظاهر زشت و وحشتناكی كه بر اثر ابتلا به این بیماری ایجاد می شود ، نجات داده است. دكتركامپیر می نویسد:
جنر واكسن خود را در پی كار طولانی و طاقت فرسا در آزمایشگاه كشف نكرد. در 19 سالگی شیردوشی به او گفته بود كه هرگز به آبله مبتلا نخواهد شد، چون قبلاً به آبله گاوی مبتلا شده بود. بعدها وقتی جنر پزشك شد و به بی فایده بودن تلاشها یش برای درمان این بیماری پی برد، جمله آن شیردوش را به خاطر آورد. تحقیق كرد و دریافت شیردوشان تقریباً هرگز، حتی وقتی از مبتلا یان به آبله پرستاری كنند، دچار آبله نمی شوند. به نظرش رسید كه آبله گاوی را به افراد تلقیح كند، تا آنها را از ابتلا به بیماری مرگبارتر آبله مصون سازد. این بخت یاری حقیقی بود. بدون این كه زحمتی بكشد، دریافت كه آبله گاوی باعث ایمنی در برابر آبله می شود. قوه تشخیص او به اندازه ای بود كه توانست به ارزش این حقیقت پی ببرد و از آن استفاده كند.
ادوارد جنر به سال 1749 در بركلی از توابع گلاسترشر انگلستان به دنیا آمد. در شش سالگی پدرش كه یك روحانی مسیحی بود ، درگذشت و برادر بزرگترش مسئولیت تربیت او را به عهده گرفت. تحصیلات ابتدایی خود را در مدارس محلی گذراند، و در آنجا به تاریخ طبیعی علاقه مند شد. تحصیل طب را زیر نظر دانیل لادلو ، از جراحان سادبری در نزدیكی بریستول آغازكرد. در این هنگام بود كه شیردوش، رابطه بین آبله گاوی و آبله را برایش تعریف كرد.
در 21 سالگی به لندن رفت تا زیر نظر پزشك مشهوری به نام جان هانتر به تحصیل ادامه دهد. دوسال در منزل هانتر سكونت داشت. در سال 1771 سرجوزف بنكس او را استخدام كرد تا نمونه های جانوری را كه در سفر اول كاپیتان كوك جمع آوری كرده بود، برایش آماده و مرتب كند. در دومین سفر اكتشافی كوك، به او پیشنهاد شد كه به عنوان طبیعیدان با آنها همسفر شود، اما جنر برای آنكه طبابت خود را در بركلی، و بعدها در چلتنهم ادامه دهد، این پیشنهاد را رد كرد. او به پرنده شناسی، زمین شناسی، موسیقی و سرودن شعر علاقه داشت، ولی در سال 1792 تصمیم گرفت علاقه خود را منحصراً به پزشكی معطوف كند و بدین ترتیب، دكترای پزشكی خود را از سن اندروز گرفت.
قاعدتاً در همین زمان بود كه خیال ایمن سازی در ذهنش نشو و نما یافت. وقتی درلندن بود رابطه بین آبله گاوی و آبله را برای هانتر مطرح كرد، اما هانتر علاقه ای به آن نشان نداده بود. در سال 1775 جنر در زمینه عقاید روستاییان گلاسترشر در باره آبله به تحقیق پرداخت. تا سال 1780 دریافت كه دو نوع آبله گاوی وجود دارد، و فقط یكی از آنها از آبله پیشگیری می كند. همچنین تعیین كرد كه نوع موثر آبله گاوی تنها وقتی اثر محافظتی دارد كه در مرحله خاصی از بیماری منتقل شود.
چون موارد آبله گاوی در منطقه سكونتش اندك بود، فرصت چندانی برای آزمودن نظریه هایش نداشت. مقداری از مایع درون تاولهای ( یا آبله ) دست شیردوشی را كه به آبله گاوی مبتلا بود بیرون كشید و آن را به لندن برد تا به پزشكان آنجا نشان دهد. اما آنان باز هم به اهمیت نظریاتش پی نبردند. با این حال، در ماه مه سال 1796 پسر هشت ساله ای را به نام جیمزفیپس با مایعی كه از تاولهای آبله گاوی دست شیردوش خارج كرده بود، مایه كوبی كرد. دو ماه بعد، با دقت ، مایع آبله را به پسرك تلقیح كرد و همان طور كه پیش بینی كرده بود، پسرك دچار آبله نشد.
انسان تعجب می كند كه چطور جنر توانست پسرك و والدینش را برای انجام چنین كار خطرناكی متقاعد كند. شاید درآن موقع همه گیری آبله در منطقه به وجود آمده بود. در این مورد یك توجیه احتمالی در مبحث ایمنی دایرة المعارف بریتانیكا( ویرایش سال 1962، جلد 12، صفحه116) آمده است: تا قبل از كشف واكسن آبله در سال 1796، مردم را با تزریق مایع به دست آمده از ترشحات پوستی مبتلایان، ایمن می كردند. برخی از افرادی كه بدین ترتیب مایه كوبی می شدند آبله می گرفتند، اما وحشت از این بیماری آن قدر زیاد بود كه بسیاری ترجیح می دادند به جای ابتلا به شكل طبیعی آبله كه اغلب اوقات كشنده بود، به بیماری تلقیح شده كه احتمال مرگ و میر بر اثر آن كمتر بود، مبتلا شوند .

نتیجه مطلوبی كه در فیپس به دست آمد برای جنر بسیار دلگرم كننده بود، اما قبل از آنكه موفقیت خود را اعلام كند، صبر كرد تا آزمایش دومی انجام دهد. این آزمایش دو سال بعد انجام شد، چون موارد آبله گاوی در گلاسترشر موقتاً به صفر رسید.
پس از دومین مایه كوبی موفقیت آمیز آبله گاوی و ایمن سازی علیه آبله، جنر برای اعلام كشفش رساله ای آماده كرد. اما تصمیم گرفت نخست به لندن برود و شیوه اش را در آنجا تكرار كند. ولی در مدت سه ماهی كه در لندن اقامت داشت كسی را پیدا نكرد كه جرئت تن دادن به مایه كوبی را داشته باشد. اما همین كه به خانه اش بازگشت، هنری كلاین كه از پزشكان برجسته بیمارستان سن توماس در لندن بود، چندین مایه كوبی را با موفقیت انجام داد، و جامعه پزشكی را از كارایی آبله گاوی در پیشگیری از آبله آگاه ساخت.
اما بروز دو مشكل متفاوت باعث شد كه پذیرش روش ایمن سازی جنر باز هم به تأخیربیفتد. از یك طرف جراح معتبری به نام ج . اینگنهاوز آن را به شدت مورد انتقاد قرار داد و برای مدتی دیگران را نسبت به آن بدبین ساخت. از سوی دیگر پزشك تندرویی به نام جورج پیرسون سعی كرد اعتبار كشف ایمن سازی را بی آنكه دانش یا تجربه ای كافی در این زمینه داشته باشد، از آن خود سازد، و ماده مایه كوبی آلوده ای تهیه كرد كه باعث بروز تاولهایی شبیه آبله می شد. جنر ثابت كرد كه واكسن پیرسون آلوده بوده است و خبر موفقیت استفاده از مایع خالص آبله گاوی به زودی در سراسر جهان منتشر شد.
فهرست زیر نشان می دهد كه در نهایت ، جنر تا چه حد مورد احترام قرار گرفت: در سال 1803 انجمن سلطنتی جنری برای گسترش شایسته ایمن سازی در لندن تأسیس شد؛ دانشگاه آكسفورد دانشنامه افتخاری دكترای پزشكی را در سال 1813 به جنر اعطا كرد؛ سالگرد نخستین ایمن سازی موفقیت آمیز ( بر روی جیمز فیپس) تا مدتها در آلمان جشن گرفته می شد؛ وزیر دارایی انگلستان 20000 پوند اعتبار در اختیار جنر گذاشت؛ هند 7383 پوند برایش كمك مالی جمع آوری كرد؛ مجسمه های جنر در گلاستر و لندن بر پا شد؛ و حتی گفته می شد كه وقتی شخص ناپلئون شنید كه جنر سفارش دو اسیر جنگی انگلیسی را كرده است، آنان را آزاد ساخت و گفت: آه، نمی توانیم خواهشی را كه بدین نام شده است رد كنیم .
اشاره:
جنر از واژه واكسیناسیون استفاده نكرد، بلكه به جایش لفظ مایه كوبی یا واریوله واكسینه را به كار برد. معنای لغوی اصطلاح لاتینی اخیر تاولهای ریز گاو است. تا حدود یك قرن بعد، مایه كوبی جنری آبله گاوی، تنها روش ایمن سازی علیه بیماری بود.در سال 1880 لویی پاستور برای ایمن سازی مرغان علیه وبا كه در یك همه گیری، 10% طیور فرانسه را از بین برده بود، روشی ابداع كرد. او باكتری ایجاد كننده این بیماری را جداسازی كرد و با كشت شكل ضعیف شده و تلقیح آن به مرغان، آنها را نسبت به حمله مرگبار بیماری ایمن ساخت. اصول كلی روش پاستور با روشی كه جنر برای مایه كوبی با آبله گاوی ابداع كرد یكی بود ( قبل از آنكه ویروس آبله به شكل آبله گاوی به شیر دوش منتقل شود، در بدن گاو ضعیف شده بود.)
در سال 1881، پاستور با روی آوردن به سیاه زخم، كه از بیماری های گاو و گوسفند است، باسیل آن را جدا كرد. او این باكتری را در دمایی بالاتر از دمای بدن حیوان كشت داد تا مایعی برای تلقیح تهیه كند كه موجب حمله خفیف سیاه زخم در جانور شود، و حیوان را برای روزی كه دچار حمله شدید بیماری می شود، ایمن سازد.
همان طور كه خود پاستور گفت، او برای ارج نهادن به شایستگی و خدمات مهم یكی از بزرگترین انگلیسیان، یعنی جنر ، واژه واكسیناسیون را به طور كلی برای روش مایه كوبی پیشگیری كننده وضع كرد.
چهار سال بعد پاستور واكسنی برای بیماری كه در حیوانات ، هاری و ( گاه ) در انسان آب گریزی خوانده می شود، ابداع كرد. پژوهشهای پیشگامانه پاستور، كه بر كشف بخت یارانه جنر مبتنی بود، ایمن سازی را به دانشی بسیار كارامد تبدیل كرد، و زمینه را برای وقوع انقلابی در مهار بیماریهای عفونی آماده ساخت. شاید گذشته از كشف آنتی بیوتیك ها، هیچ اكتشافی چنین تأثیر عمیقی بر سلامت انسان نگذاشته باشد. به نوشته و.ر. كلارك در پایه های تجربی ایمنی شناسی معاصر(1986) ، سرآمد موفقیت ها در فرایند ایمن سازی ریشه كنی كامل آبله بوده است. در نیمه نخست قرن بیستم ، سالانه حدود 2تا3 میلیون مورد جدید گزارش می شد. در سال 1949 آخرین مورد آبله در ایالات متحده، و در سال 1977 آخرین مورد تأیید شده سراسر جهان در سومالی گزارش شد.
منبع : سرگذشت اكتشافات تصادفی در علم- ترجمه : محی الدین غفرانی-
منبع:http://www.tebyan.net
تاریخچه علم ویروس شناسی
- این ذرات اساسا با کلیه میکروبهایی که شناخته شده، از نظر ساختمان و چرخه زندگی تفاوت دارند.
گرچه برای اغلب عفونتهای باکتریایی داروهای متعددی در دسترس قرار دارد ولی برای بیشتر عفونتهای ویروسی داروی موثری وجود ندارد و از اینرو ویروسها در اغلب کشورها بیماریهای تهدید کننده حیات انسان ایجاد میکنند.
- به احتمال زیاد ، ویروسها با برخی از انواع سرطانها در انسان رابطه دارند.
علم ویروس شناسی ، پس از استفاده از واکسن آبله توسط ادوارد بوخنر (1798) ، تهیه واکسن علیه بیماری هاری بوسیله پاستور (1884) و انتقال بیماری موزائیک توتون از گیاه آلوده به گیاه سالم توسط مایر در سال 1886 آغاز شده است. در سال (1892) ایوانوسکی ، ثابت کرد که عامل مولد بیماری موزائیک توتون از صافیهای بسیار ریز نگهدارنده باکتری عبور میکند. ولی نتوانست به اهمیت مساله پی ببرد. تا این که بیچرنیک (1898) دانشمند هلندی که باید او را پدر ویروس شناسی به حساب آورد ادعا کرد که عامل بیماری موزائیک توتون ، باکتری نیست و عامل مسری دیگری است. استنلی در سال 1935 با استفاده از روشهای جدید خالص کردن پروتئینها ، ویروس را خالص کرد و به پاس این خدمت ، موفق به دریافت جایزه نوبل شد.
سخن
شمشیرها، ونیزه ها وتیرها وخدنگها ، سلاحهای صنعتی وحتی مواد منفجره ی قوی، به مراتب کمنر از شپش تیفوس، کک طاعون وپشه تب زرد بر سرنوشت ملت ها تاثیر دارند. تمدنهایی بوسیله قدرت بیماری مالاریا مضمحل شده اند وارتش های انبوهی در حملات سخت اسپیریل وبا یا اسهال خونی یا باسیل حصبه شکست خورده اند. مناطق وسیعی توسط تریپانوزوم که بر بالهای مگس تسه تسه سفر می کند، ویران شده اند...جنگ...پیروزی... وتمدن صرفاً زمینه هایی را برای بروز وظهور این عوامل قدرتمند فاجعه زای بشری مهیا نموده است.
زینسر 1934
Pathology of Malaria
The most pronounced changes related to malaria involve the blood and the blood-forming system, the spleen and the liver. Secondary changes can occur in all the other major organs, depending on the type and severity of the infection. The pathological changes are more profound and severe in case of P. falciparum malaria.
Red blood cells: Red blood cells are the principal sites of infection in malaria. All the clinical manifestations are primarily due to the involvement of red blood cells.
The growing parasite consumes and degrades the intracellular proteins, mainly hemoglobin. The transport properties of the red cell membrane are altered, cryptic surface antigens are exposed and new parasite derived proteins are inserted. The red cell becomes more spherical and less deformable. In P. falciparum infection, membrane protuberances appear on the red cell surface in the second 24-hour of the asexual cycle. Accretions of electron-dense, histidine-rich parasite proteins are found under these 'knobs'. These knobs extrude a strain specific, adhesive variant protein of high molecular weight that mediates red cell attachment to receptors on venular and capillary endothelium, causing cytoadherence. P. falciparum infected red cells also adhere to uninfected red cells to form rosettes. Cytoadherence and rosetting are central to the pathogenesis of P. falciparum malaria, resulting in the formation of red cell aggregates and intra vascular sequestration of red cells in the vital organs like the brain and the heart. This further interferes with the microcirculation and metabolism and allows parasite development away from the principal host defense, splenic processing and filtration. As a result, in P. falciparum malaria, only younger forms of the parasite are found in the peripheral circulation and the peripheral parasitemia is usually an underestimate of the true parasite load. Mature forms of P. falciparum are rarely seen in the peripheral blood and when found, indicate severe infection. Sequestration does not occur in cases of P. vivax and P. malariae infections and therefore, all stages of the parasite can be seen in the peripheral blood and complications are very rare.
Anemia is a fairly common problem encountered in malaria and it poses special problems in pregnancy and in children. It can be due to multiple causes. Repeated hemolysis of infected red cells is the most important cause for a reduction in hemoglobin levels. Anemia depends on the degree of parasitemia, duration of the acute illness and the number of febrile paroxysms. It may occur even after 3-5 febrile paroxysms. P. vivax predominantly invades young red cells and the number of parasites infected rarely exceeds 2%. P. malariae develops mostly in mature red cells and the parasitemia is rarely greater than 1%. P. falciparum affects red cells of all ages and the parasitemia can be as high as 20-30% or more. Massive destruction of red cells accounts for rapid development of anemia in P. falciparum malaria. Immune and non-immune hemolysis of non-infected red cells, increased splenic clearance of parasitized as well as non-parasitized red cells, reduction of red cell survival even after disappearance of parasitemia, dyserythropoeisis in the bone marrow, drug induced hemolysis etc. can also contribute to the anemia. Some of these mechanisms may perpetuate anemia even after completion of the treatment.
Anemia of malaria is usually normocytic hypochromic with increase in the number of reticulocytes and polychromatophils. Rarely, atypical manifestations like macrocytic anemia or pseudoaplastic picture with pancytopenia may be seen. Anemia may be associated with hyperbilirubinemia of the indirect type, due to the hemolytic process. Splenomegaly may also be seen.
Leukocyte count is usually low to normal in most cases of malaria. Increased leukocyte count indicates either a severe infection or secondary bacterial infection. Reduction in the leukocyte count is attributed to hypersplenism or sequestration in the spleen. Relative lymphocytosis, monocytosis, eosinopenia, presence of stab neutrophils are observed with prolonged duration of the illness.
Thrombocytopenia is also fairly common in malaria. It has been observed that the platelet count shows a moderate decline during the paroxysms of fever. Thrombocytopenia may be related to the sequestration of the platelets in the spleen. Severe thrombocytopenia however indicates severe infection and may herald bleeding syndromes.
Erythrocyte Sedimentation Rate is usually elevated in malaria up to 30-50 mm in one hour. Prolonged malaria, severe anemia and severe malaria are usually associated with a higher ESR.
Bone marrow may show evidence of dyserythropoeisis, iron sequestration and erythrophagocytosis in the acute phase of falciparum malaria. Maturation defects may be present in the marrow for 3 weeks after the clearance of parasitemia. Large, abnormal looking megakaryocytes have been found in the marrow and the circulating platelets may also be enlarged, suggesting dysthrombopoeisis.
Spleen plays an important role in the immune response against malarial infection and splenectomy invariably activates a latent infection. Enlargement of the spleen is one of the early and constant signs of malarial infection. Spleen may become palpable as early as the first paroxysm.
Spleen may be palpable at the early stages of infection in the right lateral position or even in supine position. Its edge is usually round and hard to palpate and it may be tender. As the disease progresses, the spleen becomes harder, less sensitive and readily palpable. In falciparum malaria, spleen may not be palpable if the patient presents very early (due to severity). Otherwise, splenomegaly is common in all types of malaria.
The early enlargement of the spleen is due to engorgement, oedema of the pulp and later due to lymphoid and reticulo-endothelial hyperplasia with an increased hemolytic and phagocytic function of the organ. Frequent relapses and re-infections lead to pulp sclerosis and dilated sinuses.
Following treatment, spleen regresses in size, usually completely, within two weeks. In cases of large, fibrotic spleen due to repeated malaria, regression is slower, but complete involution with treatment is common.
Rapid and considerable enlargement of spleen may sometimes result in splenic rupture, which is a serious complication of malaria. This is more common in primary attack of malaria. Due to fibrosis and perisplenitis, rupture is less likely in case of chronic splenomegaly.
A small proportion of adults in Africa and
Enlargement of the liver also occurs early in malaria. The liver is enlarged after the first paroxysms, it is usually firm and may be tender. It is oedematous, coloured brown, grey or even black as a result of deposition of malaria pigment. Hepatic sinusoids are dilated and contain hypertrophied Kupffer cells and parasitized red cells. Small areas of centrilobular necrosis may be seen in severe cases and these may be due to shock or disseminated intravascular coagulation. Prolonged infection may be associated with stromal induration and diffuse proliferation of fibrous connective tissue. However, changes of cirrhosis are not seen. In falciparum malaria, in addition to the involvement of the mesenchyma, the hepatocytes may also be involved, causing functional changes as well (malarial hepatitis).
Malarial hepatitis is characterized by hyperbilirubinemia with elevation of conjugated bilirubin, increased levels of transaminases and alkaline phosphatase. Being part of the severe falciparum infection, it may be associated with renal failure, anemia or other complications of falciparum malaria. Liver involvement in severe falciparum malaria is due to impairment of local microcirculation associated with hepatocellular damage.
In patients with repeated attacks of malaria, liver also enlarges significantly along with a large and hard spleen. However, there is no functional abnormality of the liver in these patients. Malaria is not a proven cause for cirrhosis of the liver.
Involvement of the lungs occurs in P. falciparum malaria and is secondary to the changes in the red blood cells and the microcirculation. Acute pulmonary oedema is an infrequent but nearly fatal complication of P. falciparum malaria, largely due to capillary endothelial lesions and perivascular oedema. Fluid overload and blood transfusion may also contribute to this problem. Pulmonary capillaries and venules are packed with inflammatory cells and parasitized red cells. The vascular endothelium is oedematous with narrowing of the lumen. Interstitial oedema and hyaline-membrane formation is also seen.
Focal or lobar pneumonia and bronchopneumonia can also complicate malaria.
Malaria is commonly associated with cardiovascular function abnormalities. The most frequent changes during a paroxysm include decrease in blood pressure, tachycardia, muffled heart sounds, transient systolic murmur at the apex and occasional cardiac dilation. Also there is peripheral vasodilation, leading to postural hypotension.
In P. falciparum malaria, there could be microcirculatory changes in the coronary vessels. The myocardial capillaries are congested with parasitized red cells, pigment laden macrophages, lymphocytes and plasma cells.
Malaria may aggravate a pre-existing cardiac dysfunction and may prove fatal to patients already suffering from significant cardiac failure or valvular obstruction.
Malaria is often accompanied by nausea and vomiting, mainly central in origin. In the acute phase, patient may have anorexia, abdominal distention, and pain in the epigastrium. Some times the abdominal colics may be so severe as to mimic acute abdomen or appendicitis. Some patients may have watery diarrhoea and the condition may mimic gastro-enteritis or cholera.
Acute colitis may be associated with malaria. Bacillary dysentery, amoebiasis, etc. may complicate malaria.
In falciparum malaria, involvement of splanchnic microcirculation can lead to ischaemia of the gut, mucosal oedema, necrosis and ulceration. This may hamper absorption. Further these changes in the gut may also lead absorption of toxins, precipitating septic shock.
Malaria can cause varied problems in the kidneys. During the acute attack, albuminuria may be seen commonly. Acute diffuse malarial nephritis with hypertension, albuminuria and oedema may also be seen rarely.
In P. malariae infection, nephrotic syndrome may be seen (Quartan malaria nephropathy). This immune complex mediated nephropathy develops weeks after the malarial illness and is characterized by albuminuria, oedema and hypertension. It may be progressive and may require treatment with steroids or immunesuppressants.
In severe P. falciparum malaria, acute renal failure may develop in 0.1-0.6% of the patients. Microcirculation disorders, anoxia and subsequent necrosis of the glomeruli and renal tubules are responsible for this serious complication. Disseminated intravascular coagulation also may cause or aggravate this problem.
Central nervous system manifestations in malaria could be due to pathological involvement of the brain, paroxysms of fever or due to the side effects of antimalarial drugs.
The febrile paroxysms are usually accompanied by head aches, vomiting, delirium, anxiety and restlessness. These are as a rule transient and disappear with normalization of the temperature.
Antimalarial drugs like chloroquine, quinine, mefloquine and halofantrine can cause various symptoms like dizziness, vertigo, tinnitus, restlessness, hallucinations, confusion, delirium or even frank psychosis, convulsions etc. Quinine can induce hypoglycemic coma. Artemisinin derivatives are known to cause brain stem dysfunction in animal studies. These factors should always be kept in mind while managing cases of malaria.
Nervous system gets involved predominantly in P. falciparum malaria and only very rarely in the other forms. Decreased deformability, increased cytoadherence and rosetting of red cells, occlusion of the microcirculation by the red cell rosettes and their thrombosis- all these result in cerebral anoxia, development of malaria granulomas and punctate haemorrhages leading to malarial encephalitis and meningoencephalitis. At autopsy, the brain is found to be oedematous; small blood vessels are congested with parasitized red cells; the surface of the brain appears leaden or plum coloured while the cut surface has a slatey-grey hue. Up to 70% of the red cells in the brain may be found to be parasitised, and many mature forms of the parasite including schizonts could be seen. In larger vessels, the parasites form a layer along the endothelium, called as 'margination'. The vascular endothelium shows pseudopodial projections, which may be in close apposition to the 'knobs' on the surface of the parasitized red cells. Numerous petechial haemorrhages are found in the white matter, proximal to the occlusive plugs in the end arterioles. Dürck's granulomata, small collections of microglial cells surrounding an area of demyelination may be seen at the site of these haemorrhages.
Refernce:www.malariasite.com
برای دریافت ترجمه بر روی ادامه مطلب کلیک کنید
شير و معرفي تركيبات آنتي باكتريال آن
مقدمه
شير بهترين غداي طبيعي شناخته شده و تنها منبع غذائي نوزاد پستانداران است. براي نوزاد انسان، شير تنها منبع غذايي براي چندين ماه اول زندگي است و در اغلب كشورها شير نقش مهمي در تغذيه بچه هاي در حال رشد دارد. شير مي تواند يك منبع ارزشمند غذايي براي افراد بالغ بويژه افراد مسن باشد. شير به خاطر دو جزء اصلي خود يعني پروتئين و كلسيم در تغذيه انسان بسيار مهم است. پروئتين شير بسادگي قابل هضم است. اما شير بعلت ويژگيها و صفات ممتاز غذايي كه دارد به سرعت در معرض آلودگيهاي گوناگون قرار مي گيرد و به سادگي باعث انتشار تعداد زيادي از عوامل بيماريزا مي گردد و چنانچه در بهداشت آن در مراحل مختلف توليد و جمع آوري و حمل و نقل، تعيير و تبديل در كارخانه توزيع و مصرف، دقت كافي مبذول نگردد ممكن است بيماريها و عوارضي را از حيوان به انسان يا از انسان به انسان منتقل نمايد
در شير خام مكانيزم دفاعي آنتي ميكروبال طبيعي به شرح ذيل مي باشد:
1- ليزوزيم
2- لاكتوفرين
3- لاكتو پراكسيداز
4- ان استيل- ال- بي- دي گلوكوزآميداز
شير گونه هاي مختلف پستانداران داراي مقادير مختلفي از فاكتورهاي آنتي باكتريال مي باشد. به عنوان مثال شير گاو داراي بالاترين مقادير لاكتوپراكسيداز مي باشد. اما مقادير جزئي از ليزوزيم و لاكتوفرين در شير گاو پيدا مي شود. در حالي كه شير انسان داراي مقادير بالاي لاكتو فرين و ليزوزيم مي باشد و برعكس مقادير لاكتو پراكسيداز در آن بسيار جزئي مي باشد. تعييرات اين پروتئينها ي آنتي باكتريال علاوه براينكه در حفاظت خود پستان گاو تاثير است بلكه همچنين مسائل مرتبط با سلامتي و بهداشتي مصرف كنندگان را تحت تاثير قرار مي دهد.
همانطور كه ذكر گرديد، شير يك منبع غذائي سالم، حاوي انرژي و پروتئين و ويتامين و مواد معدني است بنابراين با توجه به اينكه ارزش غذائي شير بالاست، متخصصان امر در افقهاي تحقيقاتي آتي خود به دنبال افزايش ايمني طبيعي شير به منظور از بين بردن پاتوژنهاي آلوده كننده اين منبع غذائي مي باشند. چرا كه حصول به چنين هدفي در كنترل بيماريهاي اقتصادي مانند ورم پستان و بخصوص در سلامتي انسان تاثير عمده خواهد گذاشت.
پروتئينهاي مختلفي در شير يافت مي شود كه در گزارشات مختلف خاصيت ميكردب كشي آنها به اثبات رسيده است به عنوان مثال ايمينوگلوبولينهاي شير از جمله پروتئينهاي دفاعي و محافظي هستند كه در انتقال آنتي بادي از مادر به نوزادان نقش آفرين هستند. ازآنجايي كه نوزاد نشخواركنندگان به علت ساختار چفت مادر قادر به اكتساب ايمني ذاتي نيستند، بنابراين ايمنوگلوبولينهاي موجود در شير مادر (آغوز) نوازد تازه متولد شده را در برابر عوامل عفوني حفاظت مي كند.
ايمنوگلوبولينها در حقيقت تركيباتي هستند كه در مراحل اوليه تولد نوزاد به عنوان سيستم دفاعي طبيعي ميزبان عمل مي نمايند. نكته جالب در اينجاست كه در پاسخ به حضور عوامل پاتوژن و باكتريها و ويروسها موجود در محيط، ايمينوگلوبولين ويژه و خاص آن پاتوژن ترشح مي شود. در نتيجه ساختار چنين ايمنوگلوبولين قادر است كه پاتوژن وارده را شناسائي كند و در از بين بردن آن با موفقيت عمل كند. غلظت ايمنوگلوبولينها در آغوز در بالاترين مقدار خود مي باشد و به مرور غلظت آن در شير كاهش مي يابد.
علاوه بر ايمينوگلوبولينها، 4 پروتئين در شير وجود دارد كه خاصيت آنتي باكتريال آن به اثبات رسده است كه در اين مقاله به طور اجمالي به معرفي و بيان وظايف آنها پرداخته مي شود.
لاكتوفرين:(Lactoferrine)
لاكتوفرين يك گليكوپروئتين متصل شونده به يون آهن مي باشد(80 كيلودالتون) كه اولين بار از شير گاو جدا شده است و متعاقبا در شير انسان نيز وجود آن به اثبات رسيده است. لاكتوفرين به مقادير مختلف از غدد ترشحي موجود در پستانداران مانند شير، بزاق، اشك و مايع مني و از بعضي از گلبولهاي سفيد ترشح مي شود. مقادير لاكتوفرين موجود در شير گاو در حالت طبيعي حدود2/0 گرم در ليتر اندازه گيري شده است. در آغوز غلظت لاكتوفرين در بالاترين حد خود يعني در حدود نيم الي يك گرم در ليترگزارش شده است. در طول دوره خشكي، غلظت لاكتوفرين در غدد ترشحي پستان شروع به افزايش مي نمايد و تا 30 روز بعد از پايان دوره خشكي اين سير افزايشي ادامه دارد.
پيك ميزان ترشح لاكتوفرين در غدد ترشحي پستان حدود 50 الي 100 گرم در ليتر پيش بيني شده است. در شير انسان و در آغوز غلظت لاكتوفرين به ترتيب در حدود 2 الي 4 گرم در ليتر و 6 الي 8 ليتر گزارش شده است.
وظايف لاكتوفرين به قرار ذيل مي باشد:
1- خاصيت آنتي باكتريال
2- دفاع عليه عفونتهاي معده اي- روده اي
3- ايجاد سينرژيسم با بعضي از ايمنوگلوبولينها . پروتئينهاي سيستم دفاعي
4- محرك رشد سلولهاي بدن حيوانات به ويژه لنفوسيتها و سلولهاي روده
علاوه بر موارد فوق، يكي از وظايف لاكتوفرين موجود در شير را كمك به جذب آهن در سطح روده مي دادنند هر چند اين ادعا هنوز از لحاظ علمي به اثبات نرسيده است.
بيشتر ميكروارگانيسمهاي و پاتوژنهاي موجود، براي رشد خود به آهن احتياج دارند فلذا لاكتوفرين با اتصال به آهن از رشد باكتريهاي نيازمند به آهن از طريق غير قابل دسترس كردن آهن جلوگيري مي كند. يك مولكول لاكتوفرين قادر است كه با دو مولكول آهن (Fe+3) متصل شود. گزارش مقالات معتبر متعدد حاكي از اين است كه لاكتوفرين داراي خصوصيات آنتي باكتريال قابل توجهي مي باشد و بر عليه باكتريهاي گرم منفي نيازمند به آهن به خصوص كلي فرمها كه از عوامل اصلي ابتلا گاو به ورم پستان هستند، وارد عمل مي شود. همچنين لاكتوفرين بر عليه تعدادي از باكتريهاي گرم مثبت مانند استرپتوكوكوس اورئوس و ليستريامونوسيتوژنز نيز عمل نموده و در از بين بردن آنها نقش آفرين مي باشد.
باكتريهاي لاكتوژنيك در معده و روده كه نياز چنداني به آهن براي ادامه فعاليت خود ندارند به طور كلي تحت تاثير لاكتوفرين قرار نمي گيرند.
اخيرا گزارشاتي دال بر تاثير لاكتوفرين در از بين بردن استرپتوكوكوس و ويبريون نيز به چشم مي خورد.ثابت شده است كه لاكتوفرين ميزان كلني هاي مونوسيتهاي ميزبان را افزايش مي دهد و باعث كاهش رشد باكتري استرپتوكوكوس اورئوس مي شود. محيط كشت هاي حاوي لاكتوفرين 95 درصد عدد كمتري را در هنگام شمارش مستقيم كلوني هاي ميكروبي از خود نشان دادند.
خوكچه هايي كه در ساعات صفر، 8 ، 20 ساعت بعد از تولد استفاده كردند حدود 74 درصد داراي ميزان زنده ماني بيشتري نسبت به گروه شاهد بودند.
در سالهاي اخير توالي كامل ژن لاكتوفرين شناسائي و در بانكهاي جهاني مورد ثبت قرار گرفته و اكنون مشخصات كامل اين ژن در دست مي باشد. ژن لاكتوفرين(LF) داراي 17 اگزون و با طولي در حدود 5/34 كيلوباز ميباشد.
لاكتوپراكسيداز(lactoperoxidase)
پراكسيداز آنزيمي است كه قادر به كشتن باكتريها از طريق انجام واكنش اكسيداتيو مي باشد. فعال شدن اين آنزيم و ترشح آن در غدد برون ريزي مانند اشك، بزاق ، بيني و برونشها و ترشحات روده اي رخ مي دهد.آنزيم پراكسيدازي كه در شير ترشح مي شود به نام لاكتوپراكسيداز معروف مي باشد. لاكتوپراكسيداز يك پروتئين دفاعي است كه در گروه ايمينوگلوبولينها قرار نمي گيرد و نقش مهمي در حفاظت سيستم پستاني بر عليه ميكروبهاي آلوده كننده اين سيستم دارد.
مقادير لاكتوپراكسيداز در شير بسيار اندك است اما در حدود 5 الي 6 روز بعد از زايمان به سرعت ميزان آن افزايش مي يابد. غلظت اين آنزيم در شير انسان تقريبا 20 برابر كمتر از شير گاو مي باشد.
لاكتوپراكسيداز به خودي خود خاصيت ميكروب كشي ندارد بهر حال اين آنزيم همراه با هيدروژن پراكسيداز و تيوسيونالات اثرات ضد باكتريالي خود را ميانجيگري مي كند.
بوسيله واكنش هيدروژن پراكسيداز و تيوسيونالات با يكديگر در حضور لاكتوپراكسيداز، تركيب جديدي تحت عنوان هيپوتيوسيونولات(Hypothiocyanate) بوجود مي آيد كه خاصيت شديد ميكروب كشي دارد و از متابوليسم باكتريها به طور معني دار جلوگيري مي كند.
ليزوزيم:(Lysozyme)
ليزوزيم يكي ديگر از آنزيمهاي موجود درشير بعضي از گونه ها بويژه در انسان مي باشد.بطوركلي دو نوع ليزوزيم وجود دارد:
نوع اول ليزوزيمي است كه عمدتا در سفيده تخم مرغ وجود دارد و تحت عنوان C- ليزوزيم معروف است و نوع دوم آن در سفيده غاز به طور عمده وجود دارد و به G- ليزوزيم معروف است.
در انسان و تك سميها نوع C ليزوزيم بيشتر مد نظر است ولي گاو تقريبا حاوي هر دو نوع ليزوزيم مي باشد. ليزوزيم خاصيت ضد باكتريال دارد و از طريق تخريب پيونهاي گلوكوسيدي بين پپيتدگليكان(جزء اصلي ديواره سلولي باكتريها) باعث از بين رفتن ديواره سلولي پاتوژنها مي شود. فعاليت ليزوزيم در شير گاو هنوز در پرده اي از ابهام است ولي غلظت بالاي آن در شير انسان(12/0 گرم در ليتر) گزارش شده است. در آغوز انسان مقادير ليزوزيم در بالاترين حد خود گزارش شده است.
ان استيل ال- بي- دي گلوكوزآميداز:(N-Acetyle-B-D-Glacosaminidase)
اين آنزيم با حرف اختصاصي(NAGase)نشان داده مي شود. اين آنزيم به عنوان يك نشانگر(انديكاتور) براي تشخيص ورم پستان مورد استفاده قرار مي گيرد.اين آنزيم در ترشحات رحمي گاو نيز يافت شده است و وظيفه اصلي آن هنوز در پردهاي از ابهام است بهر حال تا حدودي خصوصيات ضد ميكروبي آن كشف شده است. در طول شيردهي، شير گاو داراي مقادير جزئي از اين آنزيم مي باشد. در موارد بروز عفونت و بخصوص در اواسط دوره خشكي پيك اين آنزيم قابل مشاهده است. در زمان بروز ورم پستان حضور اين آنزيم در محل عفونت قابل مشاهده مي باشد.
مطالعات متعدد نشان مي دهد كه فعاليتهاي باكتريهاي:
Actionmyces pyogenes
Staphylococuse aureus
Streptococcus agalactia
Psendomonas aeroginosa
برعكس اين آنزيم بر دو باكتري
Escherichia coli
Enterobacter aerogens
بي تاثير است.
جنبه هاي كاربردي قضيه:
تركيبات آنتي باكتريال كاربردهاي مهمي در توليد حيوانات شيري و توليدات حاصل از توليد و وضعيت سلامتي انسان دارند. براساس خصوصيات كاربردي و فيريولوژيكي لاكتوفرين، بعضي از ايده هاي كاربردي استفاده از اين پروتينهاي محافظ طبيعي ايجاد مي شود:
سلامتي غذا و نوشيدنيهاي حاوي لاكتوفرين و مواد نيروزا براي ورزشكاران در حال توسعه است و لاكتوفرين در فرمولاسيون شير خشك و غذاي بچه مورد استفاده قرار مي گيرد. فعاليت محدود ليزوزيم موجود در شير گاو در هنگام ابتلا به ورم پستان افزايش مي سابد.
حرارت شير گاو در حدود 75 درجه به مدت 15 دقيقه باعث كاهش 25 درصدي فعاليت اين آنزيم مي شود بهر حال ليزوزيم موجود در شير انسان نسبت به گاو در مقابل حرارت پايداري بيشتري دارد.
ليزوزيم قادر به محدود كردن مهاجرت نوتروفيلها به طرف بافتهاي عفوني مي شود . به عنوان يك تركيب ضدعفوني كننده شناخته شده است.
خصوصيات آنتي باكتريال سيستم لاكتوپراكسيداز نيز كاربردهاي زيادي در دامپزشكي و توليدات دامي پيدا كرده است.
نبود سيستم خنك كننده و يخچال در بسياري از مزارع چيني باعث شده است كه ضايعات شير در طول مدت حمل و نقل و ذخيره شير از معضلات اساسي صنعت پرورش گاوشيري در چين باشد.
دانشمندان چيني به دامداران آموزش مي دهند كه چگونه از سيستم لاكتوپراكسيداز در جهت نگهداري شير نهايت استفاده را نمايند.بطوري كه افزودن مقادير كمي از تي.سينولات سديم و پركربنات به شير خام و تازه دوشيده شده ، بطور موثر باعث كاهش معني دار شايعات شير مي شوند.
با يك هزينه نازل و با افزودن 10 درصد از اين دو ماده به 100پوند شير ، ضايعات شير كاهش مي يابد بدون اينكه در مزه شير تعيير محسوسي ايجاد شود و يا عوارض جانبي خاصي به همراه داشته باشد.
از ديگر كاربردهاي عملي مي توان به افزودن لاكتوپراكسيداز به شير جايگزين گوساله به عنوان جانشين مناسبي براي آنتي بيوتيك اشاره كرد. عملكرد بهبود يافته گوساله، بوسيله فعال شدن سيستم پراكسيداز ثابت شده است.
فعاليت ليزوزيم باعث محدود كردن مهاجرت نوتروفيلها به بافتهاي آسيب ديده مي باشد.امروزه ليزوزيم را به عنوان يك افزودني در بيمارستان در غذاي بچه بكار مي برند.تحقيقات محدودي هم نشان مي دهد كه ليزوزيم باعث كاهش عفونتهاي معده اي و روده اي مي گردد.
1. Refernce:
1- D J Grant, H Shi and C T Teng.2003. Tissue and site-specific methylation correlates with expression of the mouse lactoferrin gene. Gene Regulation Group, Laboratory of Reproductive and Developmental Toxicology, National Institute of Environmental Health Sciences, National Institutes of Health, Research Triangle Park,North Carolina 27709, USA.
2-Masako Moriuchi and Hiroyuki Moriuchi.2003. A Milk Protein Lactoferrin Enhances Human T Cell Leukemia Virus Type I and Suppresses HIV-1 Infection1.
3- Kenzo Kai, Ken-ichi Komine, Yumiko Komine, Toshinobu Kuroishi,
Tomoyuki Kozutsumi, Jin Kobayashi, Minoru Ohta4, Hajime Kitamura, and Katsuo Kumagai.2002. Lactoferrin Stimulates A Staphylococcus aureus Killing Activity of Bovine Phagocytes in the Mammary Gland. Microbiol. Immunol., 46(3), 187―194,187.
4- BEN BERKHOUT ,RE FLORIS,ISIDRA RECIO ,SERVAAS VISSER.2003. Antibacterial effects of the milk protein lactoferrin. Department of Human Retrovirology,
5- LYNN EDDE, RONALDO B. HIPOLITO,FREDA F. Y. HWANG,DENIS R. HEADON, ROBERT A. SHALWITZ, AND MICHAEL P. SHERMAN.2001. Lactoferrin protects neonatal rats from gut-related systemic infection. Am J Physiol Gastrointest Liver Physiol 281: G1140–G1150, 2.
6- HM Seyfert, A Tuckoricz, H Interthal, D Koczan, and G Hobom.1994
Structure of the bovine lactoferrin-encoding gene and its promoter.
Gene, June 10, 143(2): 265-9.
7- HM Seyfert and C Kuhn .Characterization of a first bovine lactoferrin gene variant, based on an EcoRI polymorphism. Anim Genet, February 1, 1994; 25(1): 54.
8-Pierce,A., Colavizza,D., Benaissa,M., Maes,P., Tartar,A.,
9-Karen J. Losnedahl, Hong Wang, Mueen Aslam, Sixiang Zou, and Walter L. Hurley.2003. ANTIMICROBIAL FACTORS IN MILK. Department of Animal Sciences Universtiy of
آرش جوانمرد
بخش بيوتكنولوژي صنايع غذايي
پژوهشكده بيوتكنولوژي كشاورزي شمالغرب و غرب كشور. http://commenting.blogfa.com
اهمیت بافت شناسی و روشهای مطالعه بافت
اطلاعات اولیه
بافت از تجمع سلولها بوجود میآید و سلولها از لایههای زایشی جنین ، منشا میگیرند. لایههای زایشی از یک زیگوت بوجود میآیند. لایههای زایشی در سه طبقه بیرونی (اکتودردم) ، میانی (مزودرم) و درونی (آندودرم) قرار گرفتهاند. اندامهایی نظیر پوست و مشتقات آن و سیستم عصبی از اکتودرم منشا میگیرند. مزودرم ، اندامهایی نظیر دستگاه گردش خون ، قلب ، دستگاه ادراری ، دستگاه تناسلی ، عضلات ، استخوانها و غضروف را میسازد. آندودرم دستگاه گوارش و غدد ضمیمه را ایجاد میکند.
بطور کلی چهار نوع بافت اصلی به نام بافتهای پوششی ، پیوندی ، عضلانی و عصبی در بدن وجود دارند. سایر بافتها در واقع اشکال تغییر شکل یافته همین بافتها هستند. با ایجاد بافتها ، اندامها شکل میگیرند و هر عضو از مجموعه چندین بافت ساخته شده است.
اهمیت بافت شناسی
یادگیری جزئیات ساختمانی ارگانها و اعضای مختلف برای فهم فعالیت فیزیولوژیک و تغییرات پاتولوژیک آنها ضروری است. بنابراین ، بافت شناسی نه تنها به عنوان علمی مستقل نمیتواند مطرح گردد، بلکه بهتر است مرتبط با سایر شاخههای علم پزشکی و به عنوان یکی از پایههای اصلی علوم پایه پزشکی ، مورد توجه قرار گیرد. بافت شناسی دو قسمت دارد:
· General Histology که در آن خصوصیات 4 بافت اصلی (پوششی ، پیوندی ، عضلانی و عصبی) بحث میشود.
· Speciales Histology که در آن خصوصیات بافتهای تخصص یافته مانند بافت خون ، بحث میگردد.
رابطه بافت شناسی با سایر علوم
یکی از نکات قابل توجه در مورد بافت شناسی این است که بافت شناسی ، پیوستگی بسیار نزدیکی با سایر علوم پزشکی و زیستی نظیر آناتومی ، جنین شناسی ، فیزیولوژی ، پاتولوژی و سیتولوژی دارد.
میکروسکوپ و لزوم استفاده از آن در مطالعات بافت شناسی
یکی از نکات قابل ذکر در مورد لزوم استفاده از میکروسکوپ ، اشاره به محدودیتهای چشم انسان در دیدن اجسام ریز است. بطوری که قدرت تفکیک (resolution) چشم انسان ، یعنی فاصله دو نقطهای که جدا از هم دیده میشوند، در حدود 0.1 میلیمتر و کوچکترین ساختمان قابل مشاهده بوسیله آن حدود 40 میکرومتر میباشد. بنابراین برای مشاهده ارگانیزمهای بسیار ریز و سلولهای تشکیل دهنده بافتها ، انسان ، نیازمند استفاده از ابزارهای کمکی برای چشم است.
متداولترین ابزار مورد استفاده برای مطالعه ساختمان بافتها و ارگانها ، میکروسکوپ میباشد. میکروسکوپهایی که در آنها از نور استفاده میشود به میکروسکوپ نوری موسوم هستند و قدرت تفکیک آنها در حدود 0.2 میکرون است. میکروسکوپهای نوری دارای انواع مختلفی میباشند که عبارتند از: میکروسکوپ نوری معمولی ، میکروسکوپ فلورسانس ، میکروسکوپ پلاریزاسیون ، میکروسکوپ زمینه تاریک و میکروسکوپ فاز متضاد. از میکروسکوپهای فوق با توجه به قابلیت هر کدام برای اهداف گوناگون استفاده میشود. در مطالعات هیستولوژیکی از میکروسکوپ نوری معمولی استفاده میشود.
آماده سازی بافت (Tissue Preparation)
برای مطالعه بافت و ارگانهای مختلف توسط میکروسکوپ باید آنها را به روش خاصی آماده کرده و به ضخامت 5 تا 10 میکرون برش داد، به این اعمال در مجموع ، آماده سازی بافت میگویند که با روشهای متعدد مانند نمونه برداری ، ثابت کردن ، آبگیری ، آغشته سازی ، قالب گیری ، مقطع گیری ، چسباندن و رنگ آمیزی انجام میگیرد.
|
|
تکنیکهای هیستوشیمیایی
ارزیابی فعالیتهای سلولی از قبیل تولید و یا میزان تولید یک آنزیم ، با استفاده از رنگ آمیزی ، به روش هیستو شیمیایی ، موسوم است. در این روش ، نه خود آنزیم ، بلکه ترکیبات حاصل از فعالیت آنزیم ، رنگ آمیزی میگردد.
تکنیکهای ایمونو هیستو شیمیایی
در این روش با تهیه آنتی بادی بر علیه اجزا تشکیل دهنده سلولی و نشاندار کردن آنتی بادی با آنزیم یا یک ماده رنگی دیگر ، میتوان پروتئینهای ویژهای را در بافتها و سلولها ، محلیابی نمود. اگر برای نشاندار کردن آنتی بادی از مواد فلورسانس استفاده شود، روش را به عنوان ایمونوفلوروسانس نیز مینامند. در روشهای فوق برای جلوگیری از غیر فعال شدن آنزیم برای فیکسه شدن ، از روشهای انجمادی استفاده میشود و برای بریدن آنها از میکروتوم ، بهره میگیرند.
میکروسکوپ الکترونی
قدرت تفکیک میکروسکوپ نوری در حدی نیست که بتوان ساختمان دقیق اجزا و ارگانلهای درون سلولی را بوسیله آن مطالعه نمود. بنابراین برای مشاهده و مطالعه ساختمانها فوق از میکروسکوپ الکترونی استفاده میشود. در میکروسکوپ الکترونی برای مشاهده بافت به جای نور از الکترون استفاده میشود که با توجه به طول موج بسیار کم پرتوهای الکترونی ، قدرت تفکیک میکروسکوپ الکترونی در حدود یک نانومتر (
چون الکترونها بوسیله چشم قابل رویت نیستند، الکترونهای ساطع شده ضمن عبور از نمونه مورد مطالعه به یک صفحه فلورسانت برخورد نموده و با فعال کردن آن موجب ظاهر شدن تصویر بافت روی صفحه فلورسانت میگردند. به همین دلیل این گونه میکروسکوپها را میکروسکوپ الکترونی عبوری گویند و تصاویر بدست آمده از این میکروسکوپ به صورت سیاه _ سفید است. در نوع دیگری از میکروسکوپ الکترونی که به میکروسکوپ الکترونی Scanning موسوم است، ویژگیهای سطح نمونهها مورد مطالعه قرار میگیرد و تصاویر حاصله به صورت سه بعدی هستند.
منبع:http://daneshnameh.roshd.ir
پل هرمان مولر" كاشف "سم د.د.ت" درگذشت
۲۰مهر برابر با ۱۲اكتبر ۲۰۰۶است. ۴۱سال پيش در چنين روزي "پل هرمان مولر" شيميدان سوييسي و كاشف "سم د.د.ت" چشم از جهان فروبست. اين سم، براي نخستين بار در ۱۸۷۳توسط يك دانشجوي آلماني سنتز شد، اما تا سال ۱۹۳۰به دست فراموشي سپرده شد تا اينكه مولر كه روي تاثير حشره كش هاي بلند -اثر( (Long-Lastingبر حشره بيد لباس ( (Clothes Mothتحقيق ميكرد دوباره آن را كشف كرد. اين سم تا سال ۱۹۷۳بطور گستردهاي در آمريكا عليه آفات كشاورزي و دامي استفاده شد و سپس استفاده از آن به دليل انباشتگي آن در در زنجيره غذائي ممنوع شد. مولر به خاطر كشف اين ماده كه براي بيش از ۲۰سال در سراسر جهان به صورت گسترده كاربرد داشت در سال ۱۹۴۸جايزه فيزيولوژي و پزشكي نوبل را دريافت كرد.
همچنين در چنين روزي در سال " ۱۹۴۳مكس ورتهايمر"، روان شناس متولد چك درگذشت.او يكي از پايهگذاران روانشناسي "گشتالت" به شمار ميرود. گشتالت، واژهاي آلماني به معناي شكل، ريخت، يا سازمان و مفهوم ضمني آن كليت و تماميت است. روانشناسان گشتالت ادراكات را كلها يا الگوهاي سازمان يافته ميدانند. روانشناسي گشتالت كه در نخستين دهههاي قرن بيستم در آلمان پديدار شد، عنوان ميكرد كه افراد مستعد هستند كه اطلاعات را به روشهاي خاصي سازماندهي كنند. منبع:http://aent.persianblog.ir
سالروز تولد آلبرت كالمت كاشف واكسن ب ث ژ
۲۱تير برابر با ۱۲جولاي ۲۰۰۶است. ۱۴۳سال پيش در چنين روزي "آلبرت كالمت"، باكتري شناس فرانسوي درشهر نيس، ديده به جهان گشود.
كالمت، شاگرد لويي پاستور و از پايهگذاران انستيتو پاستور شهر ليل بود.
واكسن معروف ب.ث.ژ، بعد از سالها مطالعه و كوشش ، توسط دو نفراز برجستهترين اطباي فرانسوي كشف شد كه كالمت يكي از آن دو محقق فرانسوي به شمار ميرود.
كالمت ، تحقيقاتي بر روي روشهاي واكسيناسيون عليه بيماريها به ويژه واكسن عليه سل به همراه همكار خود "كادميل گرين" انجام داد.
بدين ترتيب، نام اين دو محقق بر روي مشهورترين واكسن بيماري سل، ب ث ژ ( BCGيا باسيل كالمت، گرين)، گذاشته شدهاست.اين دو محقق روز بيست و پنجم ۲۵ژوئن ۱۹۲۴واكسن سل ( (BCGرا تكميل كردند.
كالمت همچنين، مطالعاتي بر روي سموم مارها و تهيه سرمهاي ضد سممار، انجام داد.
۱۲جولاي ۱۸۱۳نيز "كلود برنارد"، فيزيولوژيست فرانسوي به دنيا آمد.
"تعيين نقش پانكراس در عمل گوارش ، بررسي عملكرد گليكوژنيك كبد و نقش اعصاب و ازوموتور در تنظيم گردش خون"، از جمله تحقيقات مهم او محسوب ميشوند.
برنارد، همچنين نقش مهمي در كاربرد روشهاي تجربي در علوم زيستي ايفا كرد.
واژگان ویروس شناسی
|
واژه لاتین |
معادل فارسی |
تعریف |
تصویر |
|
bacteriophage |
ویروس باکتریایی |
ویروسی که در درون سلول باکتری تکثیر مییابد. |
|
|
Capside |
کپسید |
غلاف پروتئینی ویروس که اسید نوکلئیک ویروس را احاطه میکند. |
|
|
Capsomer |
کپسومر |
واحد کوچک پروتئین تشکیل دهنده کپسید |
|
|
Latent viral infection |
|
شرایطی که در آن ویروس در درون پیکر میزبان مدت زمانی بدون تولید بیماری باقی میماند. |
|
|
naked virus |
ویروس برهنه |
ویروسی که فاقد پوشش است. |
|
|
Prophage |
پروفاژ |
DNA فاژی که در DNA سلول میزبان وارد شده است. |
|
|
Provirus |
پروویروس |
DNA ویروسی که در آن DNA سلول میزبان وارده شده است. |
|
|
Slow virus infection |
|
فرایند بیماری که به تدریج طی مدت طولانی بوسیله ویروس پدید میآید. |
|
|
viremia |
ویرمیا |
اصطلاحی که برای اشاره کردن بوجود ویروسها در خون استفاده میشود. |
|
|
virion |
ویریون |
ذره ویروسی کامل |
|
|
viral hemagglatination |
|
توانایی برخی از ویروسها به آگلوتینه کردن گویچههای سرخ خون |
|
|
viropexis |
|
فرایندی که حل آن یک سلول حیوانی ، ویروس کامل را در بر میگیرد. |
|
|
Anticore=Antibody |
پادتن |
موادی که در سلول میزبان در اثر ورود ویروسها به بدن توسط دستگاه ایمنی بدن تولید میشود. |
|
|
Antibiotic |
پادزی |
موادی که برای مقابله اثرات میکروارگانیسمها از جمله ویروسها بکار میروند. |
|
|
Transformation |
ترانسفورماسیون |
تغییرات وراثتی که در سلولهای جانوری کشت داده شده، توسط برخی از ویروسها و یا مواد تومورزا بوجود میآید. |
|
|
Heamagglutination |
هم آگلوتیناسیون |
ویروسهای دارای پوشش خاردار باعث تشکیل پل بین گویچههای قرمز خون میشوند که توده حاصل هم آگلوتیناتیناسیون نام دارد. |
|
|
plaque forming units |
واحدهای سازنده پلاک |
درمحیط کشت حاوی مخلوط باکتری و ویروس ، هر پلاک نشاندهنده محل یک ویروس است. |
|
|
cytopathic effect |
اثر سایتوپاتیک |
تخریب شدن سلولهای لایهای در محیط کشت سلولهای حیوانی در اثر تکثیر ویروسها |
|
|
Eclips period |
مرحله اختفا |
زمانی که در جریان تکثیر ویروسها ، ذرات ویروس آلوده کننده مشاهده نمیشوند. |
|
|
Lytic cycle |
چرخه لیتیک |
رویدهای متوالی تکثیر فاژهای T جفت که شامل متلاشی شدن سلول میزبان بعد از رها شدن فاژها است. |
|
|
Lysognic |
لیزوژنی |
وارد شدن DNA فاژ به سلول میزبان و بدون متلاشی کردن آن |
|
|
Lysogenetic |
لیزوژنتیک |
فاژهایی که بعد از ورود به سلول میزبان مدتی را به صورت خفته میمانند. |
|
|
viroid |
ویروئید |
قطعات بسیار کوتاه RNA برهنه و فاقد غلاف پروتئینی هستند که به آنها ویروس مانند گفته میشود. |
|
|
Interferon |
انترفرون |
مادهای است که توسط سلولهای آلوده شده به ویروس تولید شود. |
|
|
virulent phage |
فاژ مخرب |
فاژی که باعث تخریب و لیز شدن باکتری میشود. |
|
|
Reverse transcription |
آنزیم ترانسی کریپتاز معکوس |
آنزیمی در تکثیر ویروسهای RNA دار دخالت دارد. |
|
|
Retrovirus |
رترو ویروسها |
ویروسهای RNA دار تومورزا |
|
|
Human immanodeficiency virus |
ویروس نقص ایمنی انسان |
این ویروس در انسان تولید بیماری ایدز میکند. |
|
|
paroviruses |
پارو ویروسها |
ویروسهای بسیار کوچک هستند که موش صحرایی و موش را آلوده میکنند. |
|
|
papova viruses |
پاپووا ویروسها |
ویروسهای کوچکی که سرطانزا هستند. |
|
|
Adeno viruses |
آدنوویروسها |
دارای اندازه متوسط بوده و باعث عفونتهای دستگاه تنفسی میشوند. |
|
|
Herpes viruses |
هوپس ویروسها |
دارای اندازه متوسط بوده و در انسان تبخال ، آبله مرغان و زونا تولید میکنند. |
|
|
Mixo viruses |
میگزو ویروسها |
دارای اندازه متوسط بوده و عامل آنفولانزای A ، B و C هستند. |
|
|
paraMixo viruses |
پارامیگزو ویروسها |
عامل پارا آنفلونزا ، سرخک و اوریون |
|
|
virus |
ویروس |
انگل سلولهای زنده ، اولترا میکروسکوپی که دارای اسید نوکلئیک محصور در غلاف پروتئینی است و قادر به زندگی در محیط غیر زنده نیست. |
|
|
plant viruses |
ویروسهای گیاهی |
ویروسهایی که در گیاهان تولید بیماری میکنند. |
|
|
animal viruses |
ویروسهای جانوری |
ویروسهایی که در جانوران تولید بیماری میکنند. |
|
|
corne viruses |
کورنا ویروسها |
این ویروسها با عفونتهای بخش فوقانی دستگاه تنفس و سرماخوردگی ارتباط دارند. |
|
|
Rabodo viruses |
رابدو ویروسها |
عامل هاری و بیماری نیوکاسل در مرغ |
|
|
rna viruses |
آرنا ویروسها |
دارای RNA تک رشتهای بوده و برخی مولد عفونتهای ویروسی هستند. |
|
|
picorna viruses |
پیکورنا ویروسها |
کوچکترین ویروسهای RNA دار |
|
|
Toga viruses |
توگا ویروسها |
شامل عده زیادی از ویروسها که بوسیله بندپایان انتقال مییابند. |
|
|
Reo viruses |
رئو ویروسها |
دارای RNA دو رشتهای و احتمالا در عفونتهای خفیف دستگاه تنفسی دخالت دارند . |
|
|
virioloid |
|
عفونت و ابتلا به ویروس آبله بدون ایجاد نشانههای شدید در شخصی که قبلا واکسینه شده است. |
|
|
virology |
ویروسشناسی |
علمی که به مطالعه ویروسها میپردازد. |
|
|
viroses |
|
بیماریهایی که توسط ویروسها ایجاد میشوند. |
|
|
virucidal |
|
به فرایندی گفته میشود که توسط آن ویروسها کشته میشوند. |
|
|
virucide |
|
به موادی که باعث از بین رفتن ویروسها میشوند. |
|
|
virulence |
ویرولانس |
به قدرت بیماریزایی ویروس گفته میشود. |
|
|
viruli ferous |
|
به میزبانی که حامل ویروس است گفته میشود. |
|
|
viruria |
|
پیدایش ویروس در ادرار |
|
|
arvor viruses |
|
ویروسهایی که توسط بندپایان منتقل میشوند. |
|
|
attenuated viruses |
|
ویروس ضعیف شده |
|
|
orphan virus |
ویروس تیم |
ویروسی است که از بافت کشت شده جدا میشود ولی در بیماری بخصوصی یافت نمیشود. |
|
منبع:http://daneshnameh.roshd.i





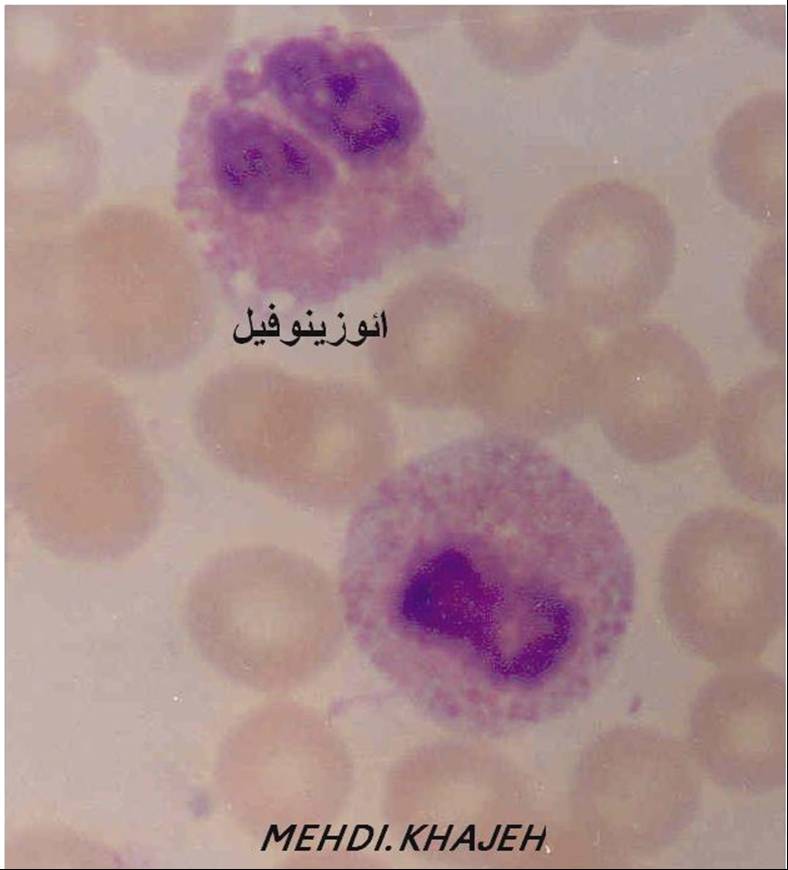

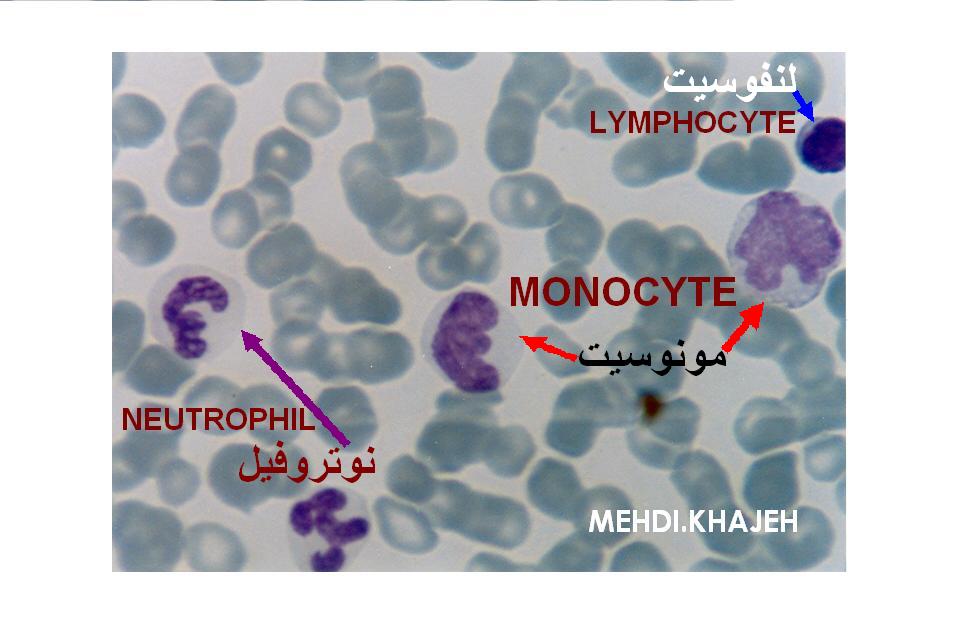
 اینجانب پیمان خادمی دانشجوی دکتری باکتری شناسی قصد دارم دراين وبلاگ مطالب مفید در مورد بیماریهای مشترک انسان و دام و همچنین در مورد محیط کشتهای میکروبی و اطلاعاتی در مورد مواد غذایی با منشا’ دامی را قرار دهم.
اینجانب پیمان خادمی دانشجوی دکتری باکتری شناسی قصد دارم دراين وبلاگ مطالب مفید در مورد بیماریهای مشترک انسان و دام و همچنین در مورد محیط کشتهای میکروبی و اطلاعاتی در مورد مواد غذایی با منشا’ دامی را قرار دهم.